Vincristine
La vincristine est un alcaloïde extrait de la pervenche de Madagascar (Catharanthus roseus) utilisé comme traitement de chimiothérapie, dans la lutte contre les cancers. Elle fait partie du groupe des poisons du fuseau mitotique, car elle inhibe la polymérisation des microtubules lors de la mitose.
| Vincristine | |
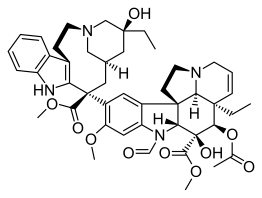
| |
| structure | |
| Identification | |
|---|---|
| Synonymes |
22-oxovincaleucoblastine |
| No CAS | |
| No ECHA | 100.000.289 |
| No CE | 200-318-1 |
| Code ATC | L01 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C46H56N4O10 [Isomères] |
| Masse molaire[1] | 824,957 6 ± 0,044 5 g/mol C 66,97 %, H 6,84 %, N 6,79 %, O 19,39 %, |
| Propriétés physiques | |
| T° fusion | 220 °C |
| Cristallographie | |
| Données pharmacocinétiques | |
| Métabolisme | hépatique |
| Demi-vie d’élim. | 19 à 155 heures |
| Excrétion |
biliaire et 10 % rénale |
| Considérations thérapeutiques | |
| Voie d’administration | Intra-veineuse |
| Grossesse | Chimiothérapie |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Historique
modifierLa vincristine est un principe actif isolé en 1965 à partir d'une fleur, la pervenche de Madagascar.
La pervenche de Madagascar, ou Cataranthus roseus, est une plante tropicale originaire de Madagascar contenant un grand nombre d'alcaloïdes, en particulier au niveau de ses racines et parties aériennes (feuilles et fleurs). Cette plante est actuellement menacée dans son milieu naturel notamment à cause de la déforestation.
Elle est depuis longtemps utilisée par les Malgaches comme « coupe-faim », vermifuge, antipaludéen, désinfectant, ou encore diurétique. En médecine traditionnelle chinoise, les extraits de cette plante sont utilisés comme traitement du diabète, du paludisme et de la maladie de Hodgkin.
En 1957, des chercheurs canadiens ont découvert de manière fortuite que l'utilisation de la pervenche de Madagascar a un intérêt pour lutter contre la leucémie. La pervenche étant connue à l'époque pour ses bienfaits sur la glycémie, ils en ont injecté un extrait sur des souris pour vérifier son action sur celles-ci. Ils n'ont alors pas observé d'abaissement de la glycémie, mais une forte diminution du taux de leucocytes. La leucémie étant associée à une surproduction de leucocytes, les extraits de pervenche apparaissent alors comme un moyen potentiel de lutte contre la leucémie.
Des chercheurs canadiens et américains, Noble et Svoboda, ont réussi à isoler la vincristine et la vinblastine à partir des feuilles de pervenche. Ces deux alcaloïdes sont utilisés actuellement pour leur activité leucopéniante.
Dans les années 1980, la société Ely&Co a été la 1re à commercialiser la vinscristine sous la dénomination Oncovin.
La vincristine est aujourd'hui le principe actif de trois spécialités commercialisées en France :
- Oncovin, 1 mg/ml sol. inj. par Eg Labo
- Vincristine Hospira, 2 mg/2 ml sol. inj. par Hospira
- Vincristine Teva, 1 mg/ml sol. inj. par Teva Santé
Pour extraire les alcaloïdes de la pervenche de Madagascar, il faut prélever les feuilles, les tiges et les fleurs de cette plante. Il est possible d'effectuer l'extraction à partir de différents solvants, parmi eux: le méthanol, le chloroforme, le dichlorométhane. À la suite d'une macération de deux semaines des composants de la plante, on évapore à sec le mélange obtenu puis on effectue une filtration à l'aide d'eau ultrapure.
La vincristine dérive d'un couplage entre deux alcaloïdes: la catharanthine et la vindoline, tous deux présents dans la pervenche de Madagascar mais en concentration plus importante que la vincristine. En effet, 1 kg de feuilles séchées de pervenche contient seulement 10 mg de vincristine contre 1 g/kg pour la vindoline et 300 mg/kg pour la catharanthine. On utilise donc préférentiellement le couplage lors de la biosynthèse et de la synthèse de la vincristine, le but étant d'obtenir le meilleur rendement. Ces deux procédés sont assez similaires.
Biosynthèse
modifierPremièrement, il y a oxydation de la catharanthine (1) à l'aide d'une peroxydase, un peroxyde (2) étant alors formé. À la suite d'un réarrangement et de l'élimination d'un hydroperoxyle HO2, la liaison entre les deux atomes de carbone est rompue ; on obtient un dication intermédiaire (3). Celui-ci va être attaqué par la vindoline (4), qui est un nucléophile par substitution électrophile aromatique. Le produit de cette réaction (5) est réduit par le NADH pour donner le cycle dihydropyridinium (6). L'étape suivante correspond à une hydroxylation. Pour finir, il y a réduction par NADH qui réduit spécifiquement l'ammonium en amine tertiaire.On obtient ainsi la vincristine.
Synthèse
modifierPremièrement, il y a oxydation de la catharantine (8) à l'aide d'acide m-chloroperbenzoïque qui conduit au dérivé N-oxyde de la catharanthine (9). À la suite d'un réarrangement et ajout d'anhydride trifluoroacétique, une liaison C-C est rompue. Un dication (10) est donc produit. Celui-ci est attaqué par la vindoline (11) qui est un nucléophile ce qui permet la substitution électrophile aromatique suivante. Sur la vindoline, le groupement méthoxy va favoriser une réaction en position ortho. Cette réaction entraîne la neutralisation de l'azote par effet mésomère. L'étape suivante est une réduction à l'aide 16'-épi-anhydrovinblastine et d'ions hydrure H-. Par ajout de chlorure de fer et d'oxygène, on réalise une oxydation qui mène au composé (14). Pour finir, du borohydrure de sodium permet la réduction sélective de l'ammonium en amine tertiaire. Le borohydrure de sodium ne réagit pas avec les autres groupements ce qui permet de les protéger. La vincristine est alors formée.
La vincristine empêche la polymérisation des microtubules en se fixant sur les dimères de tubuline libre, comme la colchicine ou la vinblastine. Cela entraîne un arrêt des mitoses et l'apoptose[6].
La mitose est une étape de la division cellulaire qui, à partir d'une cellule mère, aboutit à deux cellules-filles. Durant cette étape, les chromosomes vont migrer le long de microtubules.
Dans l'organisme, la vincristine agit sur le fuseau mitotique durant la métaphase en se liant à une protéine : la tubuline. La tubuline est un hétérodimère composé de tubuline alpha et de tubuline beta. Ces deux constituants se polymérisent pour donner des microtubules et le fuseau mitotique durant la division cellulaire. Les microtubules sont également capables de se dépolymériser pour donner des tubulines "libres". Ainsi, il y a un équilibre entre la quantité de tubulines "libres" et de microtubules.
Les alcaloïdes provenant de la pervenche de Madagascar comme la vincristine sont des poisons de la mitose. Sous l'action de ces alcaloïdes, les cellules cancéreuses qui par nature se multiplient anarchiquement sont dans l'incapacité à se diviser. En effet, la vincristine va empêcher la polymérisation de la tubuline et donc empêcher la formation du fuseau mitotique, composant indispensable à la migration des chromosomes dans les cellules filles. Elle va également induire une dépolymérisation accrue des microtubules déjà formées et inhiber l'hydrolyse de GTP. Le GTP est indispensable pour une polymérisation correcte de la tubuline. Les cellules étant dans l'incapacité à se diviser entrent en apoptose.
La vinscristine a plusieurs mode d'action:
- elle peut se lier sur un site spécifique de la tubuline et former un complexe tubuline-vinca-alcaloïde
- elle peut se lier à un site de haute affinité de la tubuline et inhiber l'ajout de tubulines
- elle peut se lier à un site de faible affinité sur le microtubule et ainsi induire la séparation du protofilament
Le test à la tubuline est un test créé par l'équipe du Professeur Potier en 1971 à l'Institut de chimie des substances naturelles. Il permet d'identifier par spectroscopie, les molécules pouvant inhiber la polymérisation des microtubules.
En règle générale, la vincristine n'affecte pas directement l'ADN. C'est un médicament antinéoplasique et antimitotique. La vincristine cible les cellules qui ont une division cellulaire rapide donc les cellules cancéreuses. Cependant, elle peut également interagir avec des cellules saines telles que les cellules de l'intestin ce qui peut engendrer des effets secondaires.
Pharmacocinétique
modifier30 minutes après l'injection, 90 % de la molécule est distribuée dans les tissus. La fixation se fait de manière réversible.
Le métabolisme de la vincristine est essentiellement hépatique. Son catabolisme au niveau des hépatocytes est assuré en majeure partie par le CYP3A4[7].
L'élimination se fait surtout par voie biliaire. La demi-vie du médicament est de 85h.
La vincristine est notamment utilisée dans le traitement des leucémies aiguës lymphoblastiques, de la maladie de Hodgkin, des lymphomes non hodgkiniens et dans un grand nombre de cancers. Il peut s'agir d'un traitement en monochimiothérapie ou en polychimiothérapie.
La vincristine est utilisée en association dans le traitement :
- des lymphomes hodgkniens et non hodgkiniens ;
- des leucémies aigües lymphoblastiques ;
- des rhabdomyosarcomes et ostéosarcomes ;
- du purpura thrombopénique idiopathique ;
- du purpura thrombotique thrombocytopénique ;
- des cancers du col de l'utérus ;
- des tumeurs embryonnaires de l'enfant ;
- des sarcomes d'Ewing ;
- des néphroblastomes (tumeur de Wilms) ;
- des neuroblastomes ;
- des myélomes ;
- des cancers du sein et du poumon.
Mode d'administration
modifierLa vincristine est une solution injectable par voie intraveineuse. Ce médicament peut être prescrit aux adultes et aux enfants, à dose variable.
En monochimiothérapie, l'injection est hebdomadaire et en polychimiothérapie, elle est mensuelle.
Une injection extraveineuse peut entraîner une nécrose des tissus. Si l'injection est faite dans le liquide-céphalo-rachidien, cela entraîne le décès ou de nombreuses séquelles.
Précautions d'emploi et contre-indications
modifierNe pas utiliser ce principe actif en cas de neuropathie, de grossesse et d'allaitement ou à la suite de certaines vaccinations. Ce médicament est déconseillé pour les patients ayant une pathologie cardiaque ou un dysfonctionnement hépatique.
La conduite après l'injection de vincristine est déconseillée à cause des effets indésirables.
Effets secondaires
modifierL'un des effets principaux est la neuropathie périphérique. Elle est moins fréquente chez les patients exprimant un type particulier de cytochrome, le CYP3A5[9] et moins rare chez ceux qui expriment un variant du gène CEP72[10].
Les effets indésirables de cette molécule sont réversibles. L'effet indésirable principal est la neurotoxicité, il peut y avoir apparition de paresthésie et de douleurs névriliques.
La constipation et les douleurs abdominales sont également fréquentes lors de ce traitement. De la fièvre, des convulsions, une hypertension et des troubles sensitifs peuvent parfois être observés.
Au niveau du système digestif, des vomissements, une perte de poids ou une perforation intestinale sont possibles.
Il apparaît rarement des œdèmes, des troubles hématotoxiques, des hyponatrémie, des ischiémies cardiaques ou dyspnée.
Un surdosage de vincristine peut entraîner une hausse de ces effets indésirables, une surveillance importante est nécessaire.
Conservation
modifierCe médicament peut être conservé au réfrigérateur, à l'abri de la lumière pendant 2 ans s'il n'est pas ouvert.
Prescription
modifierIl s'agit d'un médicament de liste I, uniquement disponible sous prescription hospitalière. Il ne peut être prescrit que par des oncologues ou spécialistes en cancérologie.
Ce traitement nécessite une surveillance médicale.
Divers
modifierLa vincristine fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[11]
Notes et références
modifier- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ « Alcaloïde »
- ↑ (en) Vincent Ting, « “The Pain Inducing, Cancer Remedy”: The Occurance, Bioactivity, Biosynthesis, and Synthesis of Vincristine », Chemistry,
- ↑ « La prevenche de Madagascar »
- ↑ « Vincristine mode d'action », sur vidal.fr
- ↑ Jordan MA, Wilson L, Microtubules as a target for anticancer drugs, Nat Rev Cancer, 2004;4:253-265
- ↑ (en) Niwa Toshiro, Yasumura Motohiro, Murayama Norie et Yamazaki Hiroshi, « Comparison of Catalytic Properties of Cytochromes P450 3A4 and 3A5 by Molecular Docking Simulation », Drug Metabolism Letters, vol. 8, no 1, , p. 43–50 (DOI 10.2174/1872312807666131229121228, lire en ligne, consulté le )
- ↑ « Vincristine, cas d'usage »
- ↑ (en) Egbelakin A, Ferguson MJ, MacGill EA et al. Increased risk of vincristine neurotoxicity associated with low CYP3A5 expression genotype in children with acute lymphoblastic leukemia, Pediatr Blood Cancer, 2011;56:361-367
- ↑ Diouf B, Crews KR, Lew G et al. Association of an inherited genetic variant with vincristine-related peripheral neuropathy in children with acute lymphoblastic leukemia, JAMA, 2015;313:815-823
- ↑ WHO Model List of Essential Medicines, 18th list, avril 2013.
Voir aussi
modifierBibliographie
modifier- Jean-Étienne Chabrier, "Molécules cytostatiques d'origine naturelle, situation actuelle, perspectives d'avenir" , Thèse de doctorat en pharmacie, Université Henri Poincaré-Nancy, 2000, p. 38-43
- (en) Vincent Ting, « The Pain Inducing, Cancer Remedy : The Occurance, Bioactivity, Biosynthesis, and Synthesis of Vincristine », Chemistry 150,
Liens externes
modifier- « La pervenche de Madagascar, remède contre le cancer », sur museum-marseille.org, (consulté le )
- « La pervenche de Madagascar », sur mediachimie.org (consulté le )
- « Pervenche de Madagascar », (consulté le )