Peroxyde d'hydrogène
Le peroxyde d'hydrogène est un composé chimique de formule H2O2. Sa solution aqueuse est appelée eau oxygénée[a]. Elle est incolore et légèrement plus visqueuse que l'eau.
| Peroxyde d'hydrogène | |
 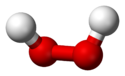  Structure du peroxyde d'hydrogène (paramètres géométriques à l'état gazeux) |
|
| Identification | |
|---|---|
| Nom UICPA | peroxyde d'hydrogène |
| Synonymes |
eau oxygénée, perhydrol |
| No CAS | |
| No ECHA | 100.028.878 |
| No CE | 231-765-0 |
| No RTECS | MX0899500 |
| Code ATC | A01, D08, S02 |
| PubChem | 784 |
| ChEBI | 16240 |
| SMILES | |
| InChI | |
| Apparence | liquide bleu pâle (à l'état pur) |
| Propriétés chimiques | |
| Formule | H2O2 [Isomères] |
| Masse molaire[3] | 34,014 7 ± 0,000 7 g/mol H 5,93 %, O 94,07 %, |
| Moment dipolaire | 1,573 ± 0,001 D[1] |
| Susceptibilité magnétique | −17,3×10-6 cm3·mol-1[réf. souhaitée] |
| Diamètre moléculaire | 0,358 nm[2] |
| Propriétés physiques | |
| T° fusion | −6 °C (10 %m), −33 °C (35 %m), |
| T° ébullition | 102 °C (10 %m), 108 °C (35 %m), |
| Solubilité | sol. dans l’oxyde de diéthyle, insol. dans l’éther de pétrole, décomposé par de nombreux solvants organiques[4] |
| Paramètre de solubilité δ | 45,9 J1/2·cm-3/2 (25 °C)[2] |
| Miscibilité | dans l'eau : miscible[5] |
| Masse volumique | 1,03 g·cm-3 (10 %m, 25 °C), 1,13 g·cm-3 (35 %m, 25 °C), |
| Pression de vapeur saturante | à 20 °C : 0,2 (90 %)[5], 0,1 (70 %) kPa[5]. 3,9 mbar à 30 °C[réf. souhaitée]. 13,2 mbar à 50 °C[réf. souhaitée] |
| Thermochimie | |
| S0gaz, 1 bar | 232,95 J/mol·K[réf. souhaitée] |
| S0liquide, 1 bar | 110 J/mol·K[réf. souhaitée] |
| ΔfH0gaz | −136,11 kJ·mol-1[réf. souhaitée] |
| ΔfH0liquide | −187,5 kJ·mol-1[réf. souhaitée] |
| ΔfH0solide | −200 kJ·mol-1[réf. souhaitée] |
| ΔvapH° | 51,6 kJ·mol-1 (1 atm, 25 °C)[6] |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 10,58 ± 0,04 eV (gaz)[7] |
| Propriétés optiques | |
| Indice de réfraction | 1,407[2] |
| Précautions | |
| SGH[9] | |
| H271, H302, H314 et H332 |
|
| SIMDUT[10] | |
   C, E, F, |
|
| NFPA 704[11] | |
| Transport | |
| Classification du CIRC | |
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[8] | |
| Inhalation | Irritation sévère, mort possible. |
| Peau | Blanchit ; nettoyer immédiatement. |
| Yeux | Dangereux ; laver immédiatement pendant un quart d'heure. |
| Ingestion | Blessure sérieuse, mort possible. |
| Autre | Plus d'infos : Hazardous Chemical Database[12] |
| Écotoxicologie | |
| DL50 | 2 000 mg·kg-1 (souris, oral)[réf. souhaitée] >50 000 mg·kg-1 (souris, i.v.)[réf. souhaitée] 1 072 mg·kg-1 (souris, s.c.)[réf. souhaitée] 880 mg·kg-1 (souris, i.p.)[réf. souhaitée] 12 000 mg·kg-1 (souris, peau)[réf. souhaitée] |
| CL50 | 2 000 mg/m3 pour 4 heures (rat, inhalation)[réf. souhaitée] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|

Le peroxyde d'hydrogène possède à la fois des propriétés oxydantes par exemple vis-à-vis d'ions iodure et des propriétés réductrices par exemple vis-à-vis des ions permanganate. C'est un agent de blanchiment efficace. Il est utilisé comme antiseptique.
Le peroxyde d'hydrogène existe naturellement chez les êtres vivants comme sous-produit de la respiration cellulaire. Tous les organismes aérobies possèdent des enzymes, appelées peroxydases, qui catalysent la dismutation de H2O2 en H2O et O2 :
La concentration des solutions de peroxyde d'hydrogène est généralement indiquée en « volumes » ou en mol/l. Par définition, 1 l d'eau oxygénée à x volumes est susceptible de dégager x litres de O2 gaz, mesurée dans les conditions normales de température et de pression, par dismutation de H2O2 (équation chimique ci-dessus). La correspondance est approximativement de 10 volumes pour 1 mol/l.
Le peroxyde d'hydrogène a été utilisé en aéronautique comme comburant (par exemple, le T-Stoff utilisé dans les années 1940 pour le Messerschmitt Me 163B), voire comme monergol pour rocketbelts dans les années 1960. Il continue à être utilisé en astronautique comme ergol oxydant, pour les vaisseaux Soyouz russes.
Transitions de phase
modifierDans les conditions normales de température et de pression, le peroxyde d'hydrogène et l'eau oxygénée sont liquides.
- l'eau oxygénée commence à bouillir à température croissante en fonction de sa concentration (de 102 °C pour 10 %m à 141 °C pour 90 %m), mais le peroxyde d'hydrogène pur se décompose, vers 150 à 152 °C[4] ;
- l'eau oxygénée commence à se congeler à température décroissante puis croissante en fonction de sa concentration (minimum voisin de −52 °C pour 50 %m), et le peroxyde d'hydrogène se congèle à −0,4 °C[4].
À l'état solide on connaît le peroxyde d'hydrogène pur (H2O2) et au moins un hydrate, H2O2·2 H2O[14].
Production
modifier- En 1992, les États-Unis en produisaient environ 348 000 tonnes. Et le Canada en produisait environ 143 000 t/an[8] ;
- En 1995, l'Amérique du Nord (Mexique y compris) avait une capacité de production estimée à 547 000 t/an[8] ;
- Pour la première moitié des années 1990, la capacité mondiale de peroxyde d'hydrogène a été estimée entre 1 800 000 et 1 900 000 t/an[8] ;
- En 2005, la capacité de production mondiale est estimée à 2 200 000 t/an[8] .
Mode de fabrication
modifierHistoriquement, le peroxyde d'hydrogène est préparé par l'électrolyse d'une solution aqueuse d'acide sulfurique ou de bisulfate d'ammonium (NH4HSO4), suivie par l'hydrolyse du peroxodisulfate S2O82− formé.[réf. nécessaire]
Actuellement, le peroxyde d'hydrogène est produit presque exclusivement par l'autooxydation de la 2-alkyl anthrahydroquinone en 2-alkyl anthraquinone (procédé à l'anthraquinone). Les industriels utilisent plus particulièrement les dérivés 2-éthyle ou 2-amyle de l'anthraquinone. La plupart des procédés industriels utilisent le barbotage d'air comprimé à travers une solution d'un dérivé dihydroxyanthracène, le dioxygène réagissant avec les protons labiles des groupes hydroxyle pour donner le peroxyde d'hydrogène, donnant ainsi le dérivé anthraquinone. Le peroxyde d'hydrogène est ensuite extrait et le dérivé anthraquinone est réduit par le dihydrogène en présence d'un catalyseur métallique pour redonner le dérivé dihydroxyanthracène, le cycle pouvant ainsi être répété[15]. Ce procédé est aussi connu sous le nom de procédé Riedl-Pfleiderer, et a été découvert en 1936[16]. En 2005, la production mondiale de peroxyde d'hydrogène atteignait 2,2 millions de tonnes[17]. La synthèse électrochimique de H2O2 à partir de l'eau et de l'oxygène est une alternative très prometteuse car elle permet: (a) la production locale là où elle est nécessaire et (b) l'utilisation de l'énergie électrique pour la synthèse chimique[18],[19],[20].
Composé naturel
modifierLe peroxyde d'hydrogène est non seulement produit par des micro-organismes mais aussi par les protéines DUOX[21],[22] ; il est ensuite détoxifié par les peroxydases afin de produire de l'hypothiocyanite[23],[24]. Il est produit naturellement par les coléoptères bombardiers et agit comme système de défense combiné à de l'hydroquinone[25]. Cette réaction exothermique libère de l'énergie et élève la température du mélange à près de 100 °C.
Décomposition
modifierLe peroxyde d'hydrogène se décompose dans une réaction exothermique de dismutation en eau et dioxygène dans des proportions dépendantes de la température, de la concentration, de la présence d’impuretés et de stabilisants. Il est décomposé par beaucoup de substances, dont la plupart des métaux de transition et leurs composés, des composés organiques, la poussière, etc. Répandre du peroxyde d'hydrogène sur une substance inflammable peut provoquer un embrasement.
L’utilisation d’un catalyseur (comme le dioxyde de manganèse, le permanganate de potassium, l'argent, ou une enzyme telle que la catalase) augmente considérablement le taux de décomposition du peroxyde d'hydrogène. Ce phénomène produit un dégagement d'oxygène intense ainsi qu'une forte chaleur. Les récipients de stockage doivent être constitués d'une matière compatible comme le polyéthylène ou l'aluminium et nettoyés de toute impureté (un procédé appelé passivation).
La réaction de dismutation est lente et les solutions aqueuses de peroxyde d'hydrogène peuvent être conservées longtemps sous certaines conditions. L'eau oxygénée commerciale dite « stabilisée » contient des agents permettant de complexer ou d'adsorber les impuretés en solution. Celles-ci catalysent la dismutation et accélèrent la décomposition de la solution, parfois violente. Pour empêcher ceci, des agents stabilisants variés peuvent être utilisés, tels des phosphates, stannates ou silicates de sodium, de l'acide phosphorique ou encore de l'acétanilide[4],[26].
La dismutation met en évidence les propriétés oxydantes et réductrices du peroxyde d'hydrogène. La dismutation peut être décrite comme une réaction entre H2O2 réducteur et H2O2 oxydant.
La réaction de dismutation
- 2 H2O2 → 2 H2O + O2 (–23,66 kcal = –98,90 kJ)
est composée des deux demi-équations d'oxydoréduction suivantes :
- H2O2 O2 + 2 H+ + 2 e− (où H2O2 est le réducteur, donneur d'électrons)
- H2O2 + 2 H+ + 2 e− 2 H2O (où H2O2 est l'oxydant, accepteur d'électrons)
Le peroxyde d'hydrogène a aussi été utilisé comme monergol. Dans les années 1930 et 1940, l'ingénieur allemand Hellmuth Walter en fut le pionnier. Cependant, son utilisation dans les torpilles a été abandonnée dans la plupart des marines pour des raisons de sécurité.
Purification
modifierComme le peroxyde d'hydrogène concentré (pourcentage molaire supérieur à 70 %) est en vente restreinte, certains sont tentés de distiller des solutions plus diluées pour obtenir un monergol. C’est extrêmement dangereux.
Le barbotage suivi éventuellement d'une congélation fractionnée constitue un procédé plus sûr. Le barbotage profite du fait que l’air tiède (pas trop chaud) évapore préférentiellement l'eau.
À des concentrations dépassant 62 %, le peroxyde d'hydrogène en solution dans l’eau gèle avant l’eau (c'est l'inverse à des concentrations plus faibles). L'eau oxygénée tend à demeurer en surfusion, un état métastable qui cesse, par exemple si l'on immerge un cristal de « glace oxygénée » dans la solution surfusée.
Toxicité, écotoxicité
modifierCe puissant biocide est toxique pour de nombreux organismes, à des doses variant selon les espèces, leur âge et le contexte. Sa toxicité a fait l'objet d'une réévaluation publiée en 1999 par le Centre international de recherche sur le cancer (CIRC)[8].
Utilisation
modifierUsage industriel
modifier- Le peroxyde d'hydrogène sert essentiellement au blanchiment de la pâte à papier (environ deux tiers du volume produit dans le monde). Les pâtes blanchies peuvent être chimiques, mécaniques ou recyclées.
- Sous une forme hautement purifiée, il revêt une importance cruciale dans l'industrie électronique (la fabrication de puces exigeant une décontamination sans faille) et les volumes produits à cet effet ne cessent d'augmenter.
- Il est utilisé dans le domaine de l'environnement pour le traitement des eaux[27], des sols et des gaz (désulfuration, deNox, dégradation de polluants aquatiques par sonocatalyse, etc.)[28],[29],[30].
- Il est contenu dans certaines solutions destinées à purifier l'eau de piscine ou de spa et détruisant les algues vertes, vendues sous l'appellation commerciale « oxygène actif ».
- La stérilisation de salles propres s’effectue par une fumigation de peroxyde d’hydrogène, par vaporisation de H2O2, ou par dispersion d’une solution en gouttelettes aérosols H2O2.
- Vaporisé à haute température, il sert à stériliser les emballages alimentaires composites juste avant l'incorporation de leur contenu (liquides UHT tels que lait, jus de fruits, etc.).
- L'oxydation d'une solution de luminol par de l'eau oxygénée produit, sans colorant, une lumière bleue intense sans dégagement de chaleur. C'est une réaction de chimiluminescence, utilisée par exemple dans les bâtons lumineux.
- C'est un oxydant prometteur pour la synthèse de différents produits chimiques[31],[32].
Usage médical ou esthétique
modifier- Naturellement sécrété par le corps humain, il inhibe la synthèse de pigments colorés, dont la mélanine, et est responsable du blanchissement des cheveux[33]. Il peut servir (à basse concentration, de 2 % jusqu'à 12 %) à décolorer les poils et cheveux, d’où l'expression « blonde peroxydée ». Il est utilisé en coiffure comme fixateur pour achever une permanente ou pour réaliser une coloration d'oxydation.
- Désinfectant pour un traitement local (code ATC : A01AB02 peroxyde d'hydrogène (eau oxygénée)). Le nettoyage des plaies par l'eau oxygénée doit être prompt, car celle-ci endommage les nouvelles cellules.
- L'Organisation mondiale de la santé (OMS) a suggéré des solutions antiseptiques pour les mains dans lesquelles l'effet antimicrobien de l'alcool hautement concentré (éthanol ou isopropanol) est renforcé par une faible concentration de peroxyde d'hydrogène tandis que le troisième composant, le glycérol, agit comme humectant. Ces formulations peuvent être préparées localement dans des endroits reculés où les désinfectants commerciaux pour les mains ne sont pas facilement disponibles. Pour ces régions, la synthèse locale de peroxyde d'hydrogène dilué a une immense importance[20].
- Combiné avec l’urée sous forme de peroxyde de carbamide H2O2·CO(NH2)2, le peroxyde d'hydrogène sert d’éclaircissant dentaire.
- Il entre dans la composition de certains traitements en dermatologie, notamment dans la kératose séborrhéique[34].
Usage en tant que comburant
modifier- À haute concentration, il peut servir de comburant pour la propulsion de fusées. En se décomposant dans le réacteur, il fournit le dioxygène nécessaire à la combustion des combustibles auxquels il est associé. Il a la particularité de pouvoir être aussi utilisé seul comme monergol (par exemple dans les Rocketbelts, ou encore dans l'avion-fusée X-15, pour les groupes auxiliaires de puissance (en anglais APU), la turbopompe et les verniers). Dans ce dernier cas, c'est la décomposition exothermique du peroxyde d'hydrogène concentré, déclenchée dans la chambre du réacteur par contact avec un catalyseur, qui produit un jet d'oxygène et de vapeur d'eau à 600 °C.
- U-boot : durant la Seconde Guerre mondiale, les équipes de l'ingénieur Hellmuth Walter expérimentèrent la propulsion des sous-marins à l'aide de peroxyde d'hydrogène comme comburant pour brûler du mazout et actionner les turbines de propulsion. Il s'agit des premiers sous-marins anaérobies jamais réalisés, permettant de s'affranchir du double système de propulsion diesel et électrique pour la surface et la plongée. Toutefois, même si les performances étaient satisfaisantes (21 nœuds en plongée soit une augmentation de 300 % par rapport aux sous-marins conventionnels), ce type d'installation propulsive était un cauchemar d'ingénieur (risques élevés d'incendie et d'explosion, immenses réservoirs, autonomie limitée) et n'atteignit pas le statut opérationnel avant la capitulation de l'Allemagne. Les coques des navires de série ayant déjà été mises sur cale furent reconverties à la propulsion classique diesel + électrique avec des capacités d'accumulateurs très importantes, donnant ainsi naissance aux redoutables U-boote Type XXI ou Elektroboote (en). Après 1945, les Anglais renflouèrent un sous-marin Walter à peroxyde (rebaptisé HMS Meteorite dans la Royal Navy), s'assurèrent de la collaboration de l'ingénieur Walter et lancèrent deux versions améliorées de cette conception, les HMS Explorer et Excalibur qui s'avérèrent extrêmement stressants pour leurs équipages (incendies spontanés, explosions, dégagements de vapeurs toxiques). Les rapports officiels les qualifiaient de « sûrs… à 75 % » tandis que les matelots les avaient rebaptisés HMS Exploder et HMS Excruciator (traduction libre : L'Explosif et Le Tortionnaire). L'avènement des sous-marins atomiques relégua ces recherches au rang de voie de garage à la fin des années 1950.
- Le véhicule terrestre supersonique Bloodhound SSC prévoit d'utiliser le peroxyde d'hydrogène comme monergol.
Autres usages
modifier- L'eau oxygénée a été utilisée durant plusieurs années comme révélateur d'hémoglobine en police scientifique. Aujourd'hui, ce test n'est plus utilisé en médecine légale car des techniques plus précises existent[35]. Cette découverte a été faite par le chimiste allemand Christian Schönbein (1799-1868). Le peroxyde d'hydrogène est utilisé pour faire réagir le luminol en utilisant le fer (II) de l'hémoglobine comme catalyseur.
- C'est aussi un désinfectant pour la culture hydroponique et l'oxygénation des racines.
- Le peroxyde d'hydrogène est aussi utilisé lors de la fabrication d'explosifs peroxydés tels que le peroxyde d'acétone (TATP).
- Associé à de l'hydroquinone, le peroxyde d'hydrogène est utilisé par les coléoptères dits « bombardiers » pour créer une solution explosive à haute température (100 °C). La solution est ensuite projetée sur ses prédateurs en tant que système défensif.
- Il fait partie des très spectaculaires réactions oscillantes de Briggs-Rauscher[36] et Bray-Liebhafsky[37],[38].
Histoire
modifierLe peroxyde d'hydrogène a été isolé pour la première fois en 1818 par Louis Jacques Thénard en faisant réagir du peroxyde de baryum avec de l'acide nitrique[39]. Le procédé a pu être amélioré en utilisant de l'acide chlorhydrique à la place de l'acide nitrique, suivi par l'ajout d'acide sulfurique pour précipiter le sulfate de baryum comme sous-produit. Le procédé Thénard est utilisé de la fin du XIXe siècle jusqu'au milieu du XXe siècle[40]. Les méthodes de productions actuelles sont discutées ci-dessous.
Le peroxyde d'hydrogène a longtemps été considéré comme instable, du fait des nombreuses tentatives pour le séparer de l'eau. Cette instabilité est due aux impuretés de métaux de transition présentes en solutions, même en très faible quantité, qui catalysent la décomposition du peroxyde d'hydrogène. Une solution pure a pu être obtenue pour la première fois par distillation sous vide en 1894 par Richard Wolffenstein[41]. À la fin du XIXe siècle, Petre Melikichvili et son étudiant L. Pizarjevski ont pu montrer que de toutes les formules proposées pour le peroxyde d'hydrogène, la formule H-O-O-H était correcte.
L'utilisation de peroxyde d'hydrogène comme stérilisant a rapidement été considérée comme une alternative efficace à l'oxyde d'éthylène et a de fait été largement utilisée dans l'industrie pharmaceutique.
Notes et références
modifier- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Hydrogen peroxide » (voir la liste des auteurs).
Notes
modifier- L'expression « eau oxygénée » ne s'applique pas au « peroxyde d'hydrogène » H2O2 pur anhydre, un liquide très instable et explosif et que l'on ne rencontre qu'extrêmement rarement (comme comburant). Ce terme de la langue courante ne concerne que les solutions aqueuses de H2O2.
Références
modifier- (en) D. R. Lide, CRC Handbook of Chemistry and Physics : 2008-2009, Boca Raton, CRC Press, , 89e éd., 2736 p., relié (ISBN 978-1-4200-6679-1 et 142006679X), p. 9-50
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, Angleterre, John Wiley & Sons, , 239 p. (ISBN 0-471-98369-1)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- N. Bonnard, M. Falcy et al., Fiche Toxicologique 123 : Peroxyde d’hydrogène et solutions aqueuses, INRS, , 8 p. (ISBN 978-2-7389-1578-8, lire en ligne)
- PEROXYDE D'HYDROGENE (SOLUTION AQUEUSE, >60 %), Fiches internationales de sécurité chimique
- (en) D.R. Lide, CRC Handbook of Chemistry and Physics, CRC Press, , 90e éd., 2804 p., relié (ISBN 978-1-4200-9084-0)
- Lide 2008, p. 10-205
- (en) IARC Monographs on the Evaluation of Carcinogenic Risks to Humans, vol. 71 : Re-evaluation of Some Organic Chemicals, Hydrazine and Hydrogen Peroxide, IARC, , 1586 p. (lire en ligne), p. 671-689
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Peroxyde d'hydrogène » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- UCB, université du Colorado
- Hazardous Chemical Database
- « Peroxyde d'hydrogène », sur ESIS (consulté le 20 février 2009).
- (en) Daniel J. Arismendi-Arrieta, Anik Sen, Anders Eriksson, Peter Broqvist, Jolla Kullgren et Kersti Hermansson, « H2O2(s) and H2O2·2H2O(s) crystals compared with ices: DFT functional assessment and D3 analysis », The Journal of Chemical Physics, vol. 159, no 19, , article no 194701 (DOI 10.1063/5.0145203 ).
- (en) J. M. Campos-Martin, G. Blanco-Brieva et al., « Hydrogen Peroxide Synthesis: An Outlook beyond the Anthraquinone Process », Angew. Chem. Int. Ed., vol. 45, no 42, , p. 6962–6984 (ISSN 1433-7851 et 1521-3773, PMID 17039551, DOI 10.1002/anie.200503779)
- Brevet US 2158525 Production of hydrogen peroxide, H. Riedl et G. Pfleiderer, 1936
- (en) R. Hage et A. Lienke, « Applications of Transition-Metal Catalysts to Textile and Wood-Pulp Bleaching », Angew. Chem. Int. Ed., vol. 45, no 2, , p. 206–222 (ISSN 1433-7851 et 1521-3773, PMID 16342123, DOI 10.1002/anie.200500525)
- (en) Luciana Vieira, « Anodic generation of hydrogen peroxide in continuous flow », Green Chemistry, Royal Society of Chemistry, vol. 24, no 20, , p. 7931–7940 (DOI 10.1039/D2GC02575B, lire en ligne, consulté le ).
- https://www.sciencedirect.com/science/article/abs/pii/S0926337321009735
- « Electrochemical synthesis of hydrogen peroxide from water and oxygen », Nat. Rev. Chem., vol. 3, , p. 442–458 (lire en ligne)
- (en) B. Rada et T.L. Leto, « Oxidative Innate Immune Defenses by Nox/Duox Family NADPH Oxidases », Contrib. Microbiol., vol. 15, , p. 164-187 (ISSN 1420-9519, PMCID 2776633, DOI 10.1159/000136357, lire en ligne)
- (en) H. Fischer, « Mechanisms and Function of DUOX in Epithelia of the Lung », Antioxid. Redox Signal., vol. 11, no 10, , p. 2453–2465 (PMID 19358684, DOI 10.1089/ars.2009.2558, lire en ligne)
- (en) P. Mowska, D. Lorentzen et al., « A Novel Host Defense System of Airways Is Defective in Cystic Fibrosis », Am. J. Respir. Crit. Care Med., vol. 172, no 2, , p. 174-183 (ISSN 1073-449X et 1535-4970, PMID 17082494, DOI 10.1164/rccm.200607-1029OC, lire en ligne)
- (en) W.E. White, K.M. Pruitt et al., « Peroxidase-Thiocyanate-Peroxide Antibacterial System Does Not Damage DNA », Antimicrob. Agents Chemother., vol. 23, no 2, , p. 267-272 (ISSN 0066-4804 et 1098-6596, PMID 6340603, lire en ligne)
- (en) T. Eisner, D.J. Aneshansley et al., « Spray mechanism of the most primitive bombardier beetle (Metrius contractus) », J. Exp. Biol., vol. 203, no 8, , p. 1265-1275 (ISSN 0022-0949 et 1477-9145, PMID 10729276, lire en ligne).
- (en) U.S. Peroxide, « Hydrogen Peroxide (H2O2) - A Powerful Oxidizer »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur h2o2.com (consulté le ).
- (en) Ainhoa Rubio-Clemente, Edwin Chica et Gustavo Peñuela, « Total coliform inactivation in natural water by UV/H2O2, UV/US, and UV/US/H2O2 systems », Environmental Science and Pollution Research, vol. 26, no 5, , p. 4462–4473 (ISSN 1614-7499, DOI 10.1007/s11356-018-3297-z, lire en ligne, consulté le )
- (en) « Design and scale-up of an oxidative scrubbing process for the selective removal of hydrogen sulfide from biogas », Journal of Hazardous Materials, vol. 215-216, , p. 49–56 (ISSN 0304-3894, DOI 10.1016/j.jhazmat.2012.02.028, lire en ligne, consulté le ).
- https://link.springer.com/article/10.1007/s11144-022-02201-1
- (en) Mohammad Hoseini, Gholam Hossein Safari, Hossein Kamani et Jalil Jaafari, « Sonocatalytic degradation of tetracycline antibiotic in aqueous solution by sonocatalysis », Toxicological & Environmental Chemistry, vol. 95, no 10, , p. 1680–1689 (ISSN 0277-2248 et 1029-0486, DOI 10.1080/02772248.2014.901328, lire en ligne, consulté le )
- (en) Lulu Xie, Hongxia Wang, Bin Lu et Jingxiang Zhao, « Highly selective oxidation of styrene to benzaldehyde over Fe3O4 using H2O2 aqueous solution as oxidant », Reaction Kinetics, Mechanisms and Catalysis, vol. 125, no 2, , p. 743–756 (ISSN 1878-5204, DOI 10.1007/s11144-018-1429-6, lire en ligne, consulté le )
- (en) Manman Jin, Zhenmei Guo, Xiaoping Ge et Zhiguo Lv, « Tungsten-based organic mesoporous SBA-15 materials: characterization and catalytic properties in the oxidation of cyclopentene to glutaric acid with H2O2 », Reaction Kinetics, Mechanisms and Catalysis, vol. 125, no 2, , p. 1139–1157 (ISSN 1878-5204, DOI 10.1007/s11144-018-1486-x, lire en ligne, consulté le )
- « On connaît la cause des cheveux blancs », Science et Vie, no 1100, , p. 21 (ISSN 0036-8369)
- Baumann LS, Blauvelt A, Draelos ZD et al. Safety and efficacy of hydrogen peroxide topical solution, 40% (w/w), in patients with seborrheic keratoses: results from 2 identical, randomized, double-blind, placebo-controlled, phase 3 studies (A-101-SEBK-301/302), J Am Acad Dermatol, 2018;79:869-877
- cf. Espace Mendès-France à Poitiers, Exposition « Police scientifique ».
- L. I. Csepei et Cs. Bolla, « Is Starch Only a Visual Indicator for Iodine in the Briggs-Rauscher Oscillating Reaction? », Studia Univ. Babes-Bolyai Chemia, vol. 2, no 1, , p. 187-200 (lire en ligne)
- (en) Nataša Pejić, Ljiljana Kolar-Anić, Jelena Maksimović et Marija Janković, « Dynamic transitions in the Bray–Liebhafsky oscillating reaction. Effect of hydrogen peroxide and temperature on bifurcation », Reaction Kinetics, Mechanisms and Catalysis, vol. 118, no 1, , p. 15–26 (ISSN 1878-5204, DOI 10.1007/s11144-016-0984-y, lire en ligne, consulté le )
- (en) Dragomir Stanisavljev, Itana Nuša Bubanja et Kristina Stevanović, « Determination of iodate ion in the presence of hydrogen peroxide with the stopped-flow technique », Reaction Kinetics, Mechanisms and Catalysis, vol. 118, no 1, , p. 143–151 (ISSN 1878-5204, DOI 10.1007/s11144-016-0977-x, lire en ligne, consulté le )
- (en) L.J. Thénard, « Observations sur des nouvelles combinaisons entre l’oxygène et divers acides », Annal. Chim. Phys., 2e série, vol. 8, , p. 306-312 (ISSN 0365-1444, lire en ligne)
- (en) C.W. Jones, Applications of hydrogen peroxide and derivatives, Cambridge, Royal Society of Chemistry, coll. « RSC clean technology monographs », , 264 p. (ISBN 0-85404-536-8 et 9780854045365, lire en ligne)
- (de) R. Wolffenstein, « Concentration und Destillation von Wasserstoffsuperoxyd », Ber. Dtsch. Chem. Ges., vol. 27, no 3, , p. 3307–3312 (ISSN 0365-9496, DOI 10.1002/cber.189402703127)
Voir aussi
modifierArticles connexes
modifierLiens externes
modifier- Fiche de sécurité.
- Fiche toxicologique de l'INRS.
- Le peroxyde d’hydrogène dans les produits de blanchiment des dents, résumé du rapport du CSPC de la Commission européenne, 2006.
- Les dangers du peroxyde d’hydrogène en stérilisation et bio-décontamination







