Benfluorex
Le benfluorex, commercialisé sous le nom de Mediator par les laboratoires Servier de 1976 à 2009[6], est un principe actif pharmaceutique, chimiquement proche de la norfenfluramine, une substance toxique elle-même très proche de l'amphétamine[5]. De 1976 à 2009, près de deux millions de personnes ont fait l'objet d'une prescription de Mediator[7].
| Benfluorex | ||
| ||
 | ||
| Identification | ||
|---|---|---|
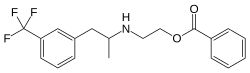
| Nom UICPA | benzoate de (RS)-2-({1-[3-(trifluorométhyl)phényl]propan- 2-yl}amino)éthyle | |
| Synonymes |
benfluramate |
|
| No CAS | ||
| No ECHA | 100.041.601 | |
| No CE | 245-777-9 | |
| Code ATC | A10 | |
| PubChem | 2318 | |
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | C19H20F3NO2 [Isomères] |
|
| Masse molaire[1] | 351,362 8 ± 0,017 4 g/mol C 64,95 %, H 5,74 %, F 16,22 %, N 3,99 %, O 9,11 %, |
|
| Écotoxicologie | ||
| DL50 | 2 300 mg·kg-1 (souris, oral)[2] 108 mg·kg-1 (souris, i.p.)[3] |
|
| LogP | 4,670[4] | |
| Données pharmacocinétiques | ||
| Biodisponibilité | 0 % | |
| Métabolisme | 1. norfenfluramine-éthanoate (ou S1475)[5] 2. norfenfluramine 3. N-(2-hydroxyéthyl)norfenfluramine (ou S422) |
|
| Excrétion |
principalement rénale des métabolites |
|
| Considérations thérapeutiques | ||
| Voie d’administration | Orale | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
La reconnaissance de la toxicité du benfluorex a conduit à l'arrêt de sa commercialisation dans plusieurs pays. En France, ce fut seulement en 2009 grâce au combat mené par Irène Frachon, pneumologue au CHU de Brest, qui a permis de révéler l'affaire du Mediator. Les autres fenfluramines, également toxiques[5], n'étaient plus commercialisées depuis 1997[8].
Le ministère de la Santé français indique que le Mediator a provoqué la mort d’au moins 500 personnes[9].
Par un arrêt du , la Cour de cassation reconnaît la responsabilité des laboratoires Servier, confirmant l’imputabilité des troubles cardio-vasculaires au Mediator :
« L'état des connaissances scientifiques ne permettait pas d'ignorer les risques d'HTAP (hypertension artérielle pulmonaire) et de valvulopathies induits par le benfluorex[10],[11]. »
Historique
modifierMise sur le marché et ventes
modifierLe benfluorex a été commercialisé de 1976 à 2009 en France par le groupe Servier, notamment comme médicament indiqué dans le traitement du diabète de type 2, dit « gras » (car associé à une surcharge pondérale). Il a également été prescrit, hors indications thérapeutiques remboursables, aux patients désireux de perdre du poids[12]. Une conséquence de la prescription hors AMM est que la remontée des informations de pharmacovigilance (effets indésirables) s'en trouve réduite, les médecins pouvant craindre — s'agissant de prescriptions hors AMM — l'engagement de leur responsabilité[13].
Les laboratoires Servier ont vendu du au « un total de 134 458 828 unités de Mediator. Ces ventes ont généré un chiffre d’affaires de près de 500 millions d’euros. Le nombre de patients traités entre 1976 et 2009 est estimé à 5 millions, avec une durée moyenne de prise du produit d’environ dix-huit mois. Trois millions de mois de traitement ont été délivrés entre 2002 et 2007. Plus de 300 000 patients s'en voyaient prescrire chaque année. Sept millions de conditionnements ont été vendus chaque année[14]. »
Affaire du Mediator
modifierÀ la suite des travaux d'Irène Frachon, le médicament a été retiré de la commercialisation en France à la fin de l'année 2009. Par la suite, Irène Frachon a lutté pour obtenir l'indemnisation des victimes du Mediator. On parle alors du scandale du Mediator[15],[16],[17].
Depuis au moins 1990, Servier savait que le benfluorex provoque l'apparition dans l'organisme de la norfenfluramine[5],[18].
En , l'Afssaps a estimé que ce médicament avait causé au moins 500 morts en France[19]. Toutefois, des chiffres plus alarmants circulent : en , une étude menée par des épidémiologistes mandatés par l'Afssaps a estimé qu'en tenant compte des décès encore à venir, le nombre de victimes du Mediator se situerait plutôt entre 1 000 et 2 000 morts[20]. Ces chercheurs de l'INSERM ont ensuite précisé leur estimation en évaluant le nombre de décès à 1 320[21],[22], ce qui impliquerait plusieurs dizaines de milliers de cas de valvulopathies, puisque seule une très faible minorité d'entre elles conduisent au décès.
L'Agence Nationale de sécurité du médicament (ANSM) a complété en une série de questions/réponses à l'intention des patients qui ont été traités par Mediator[23].
Une étude publiée le , fondée sur les demandes d'indemnisation et s'appuyant donc sur des cas réels et non des estimations statistiques, aboutit à des chiffres moins élevés. Sur un échantillon représentatif de 1 784 dossiers étudiés par le collège d'experts de l'ONIAM, 293 avis sont potentiellement imputables au Mediator. En extrapolant ces 293 cas à l'ensemble des dossiers examinés par l'ONIAM, le nombre de valvulopathies (ce qui ne signifie pas de décès) liées au Mediator devrait être revu à la baisse[24].
L'affaire du Mediator se conclut par la condamnation de Servier et de l'Agence du médicament en , puis par une seconde condamnation du laboratoire en appel en 2023. Les dommages imputables à un traitement par Benfluorex font partie des dommages pouvant être indemnisé sur saisine directe.
Chronologie détaillée
modifier1960-1980
modifier- 1960 : Albert Weissman et al. (1960) publient au congrès de la Société américaine de pharmacologie et de thérapeutique un article sur la norfenfluramine. Sa pharmacologie se caractérise par un effet anorexigène sans stimulation notable du système nerveux central. Les auteurs concluent : “ P-1727 (code de l'analogue parasubstitué de la norfenfluramine) retains much of the anorectic potency of amphetamine in rats without concomitant behavioral stimulation, as measured by operant conditioning techniques”. Ensuite, le développement de composés trifluorés de la phényléthylamine va donner naissance au groupe des fenfluramines, avec notamment la fenfluramine, la D-fenfluramine et le benfluorex.
- 1967 : Laszlo Beregi et al. (groupe Servier) déposent une demande de brevet aux États-Unis couvrant le benfluorex (notamment pour ses propriétés anorexigènes observées chez l'animal)[25]. Un brevet sera également délivré dans différents pays européens dont la France[26].
- 1970 : Jacques Duhault et C. Malen (groupe Servier) présentent le benfluorex, un nouveau dérivé des fenfluramines[27].
- 1971 : L'OMS attribue le nom de benfluorex au composé SE780 du groupe Servier[28], le suffixe « -orex » étant le suffixe généralement attribué par la nomenclature de l'OMS aux agents anorexigènes[29], mais il existe des anorexigènes dont la DCI ne se termine pas par « -orex » : amphétamine, fenfluramine, phentermine[30].
- Publication d'une étude sur « l'épidémie » d'HTAP survenue en Suisse à la suite de l'utilisation d'aminorex, un coupe-faim[31].
- 1973 : Servier demande à l'OMS que le benfluorex ne soit plus désigné comme un anorexigène, mais soit renommé « benzaflumine » ou « benflurate ». La demande est rejetée[32].
- 1974 : Goudie et al. (Psychopharmacologia) confirment chez le rat les propriétés anorexigènes de la norfenfluramine ; ils concluent qu’une partie au moins des effets de la fenfluramine est due à celle de son métabolite principal la norfenfluramine : « The data reported in this paper provide evidence which implicates norfenfluramine as a mediator of the actions of fenfluramine »[33].
- En France, le ministère de la Santé accorde l'autorisation de mise sur le marché (l'AMM) au benfluorex, non pour son action anorexigène, mais comme « adjuvant » au régime alimentaire, dans deux indications : hypertriglycéridémies et diabète chez les patients en surcharge pondérale[5]. (En , deux anciens chercheurs du laboratoire Servier, Jean Charpentier et Jacques Duhault, déclareront aux juges que les caractéristiques anorexigènes du Mediator, du fait de sa nature amphétaminique, ont été cachées pour en faire un antidiabétique, afin de faciliter l'obtention de l'AMM[34].)
- 1976 : Mise sur le marché du benfluorex sous le nom commercial de Mediator dans deux indications : hypertriglycéridémies en complément d'un régime, et chez les diabétiques en surpoids[27].
- 1976 : Un article de la revue Pratiques souligne que le Mediator est un dérivé de l’amphétamine et que cette caractéristique, peu mise en évidence par Servier, doit être connue des prescripteurs, afin de surveiller les réactions des malades. L'article conclut : « Dans quelques années, quand on commencera à savoir un petit bout de la vérité, ça en fera déjà des millions de boîtes de Mediator vendues [35]! » La revue Pratiques ou les cahiers de la médecine utopique, du Syndicat de la médecine générale, publie à nouveau un article critique de 3 pages, en 1977[36].
- 1977 : Servier dépose une demande d'autorisation de mise sur le marché belge pour le benfluorex. Après évaluation du dossier, la Commission des médicaments belge émet un «avis défavorable» du fait de l'insuffisance de données relatives aux effets à long terme du médicament. Servier fait appel de cette décision[37].
- 1977 : Henri Pradal, médecin et coauteur du Dictionnaire critique des médicaments, édition 1977-1978, souligne la proximité des formules du Mediator et du Pondéral, et son absence d'efficacité attendue. (ref : rapport IGAS).
- 1978 : La Commission des médicaments belge confirme son « avis défavorable ». L'Inspection générale de la pharmacie belge écrit que « les nouvelles données cliniques fournies (…) ne permettent pas de considérer que le produit exerce une activité hypolipidémiante ou hypoglycémiante. » La Commission évoque également « l'effet anorexigène de la molécule[37]. »
1981-1991
modifier- : Publication de deux cas ("strong evidence") d'hypertension artérielle pulmonaire sous fenfluramine[38].
- 1988 - 1991 : La littérature scientifique fait état de ce que certains des effets principaux et secondaires de la fenfluramine (Pondéral) sont dus à son métabolite N-désalkylé, la norfenfluramine[39],[40],[41]. Le laboratoire fabricant, Servier, a connaissance du fait que le Mediator (benfluorex) donne chez l'humain ce même métabolite, la norfenfluramine, à des concentrations voisines de celles mesurées après administration de Pondéral[42].
1993-1999
modifier- 1993 : Publication par François Brenot et al. d'une étude rétrospective établissant le risque d'hypertension artérielle pulmonaire (HTAP) sous fenfluramine[43].
- 1995 : À l'occasion d'une enquête sur les anorexigènes (coupe-faim), le comité de pharmacovigilance interdit le benfluorex dans les préparations magistrales[44],[45].
- 1996 : Publication des résultats de l'enquête IPPHS (International Primary Pulmonary Hypertension Study) demandée par les laboratoires Servier au professeur Lucien Abenhaïm, laquelle démontre le risque des anorexigènes du type de la fenfluramine, sans mentionner le benfluorex[46]. Malgré cette étude, l'Isoméride est autorisé par la FDA aux États-Unis, en raison de l'importance du problème de l'obésité. Lucien Abenhaïm dit ne pas avoir été au courant à l'époque de la proximité entre le Mediator et la fenfluramine.
- 1997 : Les fenfluramines, en particulier l'Isoméride, sont rendues responsables aux États-Unis de valvulopathies cardiaques ainsi que d'hypertension artérielle pulmonaire (HTAP) et sont interdites sur l'ensemble du territoire des États-Unis, ainsi que dans la plupart des pays de l'Union européenne[27]. Aux États-Unis, près de quatre milliards de dollars d'indemnisation seront obtenus lors de « class actions ». La France suspend l'AMM de l'Isoméride[44].
- 1997 : Une enquête de pharmacovigilance sur le benfluorex est lancée en France. En effet, le médicament est détourné comme anorexigène, et son métabolisme donne le même composé toxique que l'Isoméride : la norfenfluramine.
- 1997 : En Suisse, le benfluorex (vendu sous le nom de "Mediaxal") est retiré du marché par l'Institut Helvétique d'Homologation et de Contrôle des Médicaments, Swissmedic[47], en raison de "doutes" sur son innocuité.
- 1998 : L'Union régionale des caisses d'assurance-maladie (URCAM) de Bourgogne montre que plus d'un tiers des prescriptions se situent hors autorisation de mise sur le marché (AMM), le Mediator ayant pris le relais de l'Isoméride comme coupe-faim[44]. Elle souligne l'association du Mediator à des traitements à visée amaigrissante : « Au-delà des aspects de santé publique liés à des prescriptions inutiles, voire dangereuses pour la santé, le constat d'une utilisation en dehors du champ des indications reconnues et valides pose également une question d'ordre économique ». Un tiers des prescriptions du Mediator (35 %) sont ainsi faites hors AMM[48].
- 1998 : La Commission d'Autorisation de Mise sur le Marché note « l'absence d'efficacité du benfluorex dans l'hypertriglycéridémie »[27]. L'utilisation du benfluorex dans les préparations magistrales est interdite en France[49].
- 1998 : L'Assurance Maladie met en garde par courrier l'Agence du médicament sur "l'utilisation non contrôlée d'un produit de structure amphétaminique, dans un but anorexigène", le Mediator (benfluorex)[48].
- : À la demande des autorités sanitaires italiennes, le Mediator fait l'objet d'une enquête au niveau européen, dont la France et l'Italie sont les rapporteurs. Les interrogations portent sur la similitude chimique entre l'Isoméride (interdit à la vente) et le Mediator (benfluorex). Aucune suite n'est donnée à l'enquête[50].
- : Dans un courrier adressé au directeur général de l'Agence du Médicament, Jean-René Brunetière, trois médecins-conseils, le Professeur Hubert Allemand, médecin-conseil de la Caisse nationale de l'assurance maladie (CNAM), le Professeur Claudine Blum-Boisgard (CANAM), le Professeur Patrick Choutet (Mutuelle Sociale Agricole) écrivent : « Il nous apparaîtrait opportun de procéder à une réévaluation de l'utilité du Mediator dans la stratégie thérapeutique de la maladie diabétique et dans celle des hyperlipidémies. » « Il nous semble utile d'alerter l'Agence du médicament sur l'utilisation non contrôlée d'un produit de structure amphétaminique, dans un but anorexigène. Il est en effet assez paradoxal de constater que la prescription de Mediator est tout à fait libre, tandis que celle des médicaments du groupe des amphétaminiques est strictement encadrée depuis »[50],[51].
- : Georges Chiche, cardiologue, déclare un cas d’insuffisance aortique chez un patient auquel il avait été prescrit du Mediator à Marseille (Centre PHV), sans suite donnée[52],[44], cette insuffisance aortique étant, par erreur, considérée comme la conséquence d'un infarctus.
- : Une patiente de l'hôpital Saint-Joseph consulte à l'hôpital Antoine-Béclère pour son HTAP. Le professeur Simonneau est alerté par la prise par la patiente de Mediator et découvre la similitude de la molécule avec l'Isoméride, qu'il a déjà contribué à faire interdire. Il alerte la pharmacovigilance.
- 1999 : La Commission de la Transparence estime l'intérêt du Mediator « insuffisant dans ses deux indications » et propose – en vain - son déremboursement[44]. Le benfluorex reste remboursé à 65 %, mais en principe réservé aux diabétiques en surpoids. Du fait de leur toxicité, tous les amphétaminiques sont retirés du marché, sauf le Mediator[27].
- : Selon un compte-rendu de la Commission Nationale de Pharmacovigilance, «Le benfluorex (dénomination commune du Mediator) a fait l'objet d'une enquête « officieuse » dès 1995 en raison de sa parenté structurale avec les anorexigènes amphétaminiques. Cette enquête est devenue officielle en .»[50]
- : Un rapport réalisé par des experts italiens (Dr Giuseppe Pimpinella et Dr Renato Bertini Malgarini) à la demande de l'Agence européenne du médicament souligne la similitude entre l'Isoméride et le benfluorex : Il existe des suspicions que les patients traités au benfluorex sont exposés à un niveau potentiellement toxique de norfenfluramine. Trois comprimés de Mediator conduisent à produire autant de norfenfluramine que deux comprimés d'Isoméride (posologies quotidiennes pour ces deux médicaments). Enfin, ils relèvent que l'activité thérapeutique du Mediator pour les obèses ayant un diabète de type 2 (non insulino-dépendant) est inférieure à celle de la metformine, un antidiabétique de référence[53].
2000-2005
modifier- 2000 :
- L. Fitzgerald et al.[54] évoquent le rôle d'un métabolite dans l'induction des valvulopathies associées à la dexfenfluramine (tout comme à la fenfluramine) : la norfenfluramine (qui est aussi l'un des deux métabolites principaux du benfluorex).
- Sur sa base de données en ligne, le Conseil national de l'Ordre des médecins (CNOM) publie près de quatre-vingts dossiers de sanctions de médecins libéraux pour mauvaise prescription du Mediator[48] : « Prescription de Mediator hors autorisation de mise sur le marché et absence d'indication sur l'ordonnance de son caractère non remboursable » ; « A prescrit du Mediator en l'absence d'hypertriglycéridémie ou de diabète avec surcharge pondérale », « A prescrit des médicaments à effet diurétique (…) en association avec du Mediator pour des personnes désireuses de maigrir (…) (associé au) caractère dangereux de ces thérapeutiques ».
- : publication d'un article mettant en évidence le rôle des récepteurs 5-HT2B dans les hypertensions artérielles pulmonaires (HTAP) et les atteintes valvulaires, et suggérant que tous les médicaments à activité sérotoninergique soient étudiés et suspendus en cas d'action sur ces récepteurs[55].
- 2002 : l'Afssaps interdit une publicité du laboratoire Servier. L'étude sur laquelle celle-ci était fondée n'était pas conforme aux dispositions de l'Autorisation de Mise sur le Marché et ne démontrait pas la valeur ajoutée du médicament[27].
- 2003 :
- : un premier cas d'insuffisance valvulaire cardiaque est décrit en Espagne[56]. La molécule est retirée par le laboratoire à la suite des questions qui lui sont posées sur sa pharmacodynamie, et avant la date prévue de son renouvellement d'Autorisation de Mise sur le Marché. Selon les autorités espagnoles, « le benfluorex a été retiré en 2003 à la demande du fabricant en raison de sa possible implication dans les valvulopathies cardiaques »[57].
- : La revue Science et Vie, dans son dossier "le guide des médicaments", décrit le Mediator comme un produit qui "s'apparente plutôt à un coupe-faim" et qui n'a "jamais prouvé son efficacité dans la prévention des complications de l'athérosclérose[58]."
- : la revue Prescrire appelle à rester vigilant vis-à-vis des dérivés amphétaminiques.
- 2004 : le Mediator est retiré du marché en Italie[57].
- 2005 :
- L'Espagne interdit les préparations médicinales à base de benfluorex, en rappelant les risques de valvulopathies[57].
- le centre de pharmacovigilance de Besançon pointe dans un rapport des cas d'hypertension artérielle pulmonaire chez des patients ayant pris du Mediator,
- la Commission nationale de pharmacovigilance considère que les cas d'hypertension artérielle pulmonaire signalés sont peu nombreux et peuvent correspondre à l'incidence des hypertensions artérielles pulmonaires idiopathiques. Elle ne mentionne pas le problème des valvulopathies. Elle propose « d'étudier la possibilité d'interroger les registres des hypertensions artérielles pulmonaires existants des dix-sept centres, afin de rechercher, dans une étude rétrospective cas-témoins, le rôle éventuel du benfluorex »[59],
- la revue Prescrire est la première publication à demander le retrait du Mediator[60],[61].
2006
modifier- 2006 : Le Mediator n’est plus commercialisé qu’au Portugal, à Chypre et en France (où deux médecins travaillant pour le laboratoire fabriquant le Mediator étaient conseillers auprès du ministre de la santé Xavier BERTRAND[62], quand celui-ci a prorogé le remboursement du médicament en 2006[63]).
- 2006 : Un cas de valvulopathie sous Mediator chez une patiente de quarante-huit ans sans antécédent est publié par le Pr Montastruc, médecin au CHU de Toulouse et membre de la Commission Nationale de Pharmacovigilance[27]. Survenant après sept notifications spontanées, cette nouvelle déclaration ne conduit pas à l'interdiction. La Commission d'Autorisation de Mise sur le Marché renouvelle l'autorisation quinquennale du Mediator, se contentant de supprimer l'une de ses indications mineures[44].
- : la revue Prescrire rapporte trente-cinq cas français de troubles psychiatriques et de dix-sept cas d'hypertension artérielle pulmonaire (HTAP) associés au Mediator[27]. Prescrire s’étonne, une nouvelle fois, du maintien sur le marché du benfluorex (Mediator) par le laboratoire Servier[14].
2007
modifier- 2007 : Servier ne demande pas le renouvellement de l'Autorisation de Mise sur le Marché du Mediator en Italie[44].
- 2007 : L'Autorisation de Mise sur le Marché est renouvelée en France (88 % des ventes mondiales de Mediator) pour le diabète, et supprimée pour l'hypertriglycéridémie. De nouvelles études sont demandées. Le dictionnaire des médicaments Dorosz mentionne le risque de valvulopathie sous Mediator.
2008
modifier- : Dans un courriel au Centre de pharmacovigilance de Brest, un des directeurs du groupe Servier déclare que le Mediator « se distingue radicalement des fenfluramines »[27].
2009
modifier- : Onze cas de valvulopathies sous Mediator sont signalés à l'Afssaps par le CHU de Brest.
- : Irène Frachon, médecin au CHU de Brest se rend à l'Afssaps à Saint-Denis, à un groupe de travail intitulé «Plan de gestion des risques et pharmaco-épidémiologie» et fait part de ses inquiétudes concernant le lien entre valvulopathies et prise de Mediator.
- : Après la réunion du à l'Afssaps, l'épidémiologiste Catherine Hill adresse un courriel à tous les experts de l'Afssaps. Elle évoque un « signal particulièrement clair » entre la prise du benfluorex et valvulopathies. Elle juge « très peu prudent d'attendre pour agir » et note que « si nous étions aux États-Unis, le risque de procès serait très élevé ». Elle rappelle que le médicament a été retiré du marché en Espagne « pour les mêmes raisons » depuis plusieurs années[64].
- : Irène Frachon se rend à la Commission Nationale de Pharmacovigilance. Il est demandé aux laboratoires Servier de faire une étude de type cas-témoins, qui peut prendre des années et nécessiter d'étudier des milliers de cas[64].
- : Selon une étude d'Irène Frachon, du CHU de Brest, « 70 % des malades souffrant d’atteintes inexpliquées de leur valvule mitrale ont été exposés à une prise de Mediator, contre 6 % chez les malades ayant une cause connue de valvulopathie »[14].
- : Nouvelle réunion à l'Afssaps avec l'équipe du CHU de Brest. Il existerait un lien très fort entre valvulopathies et prise de Mediator[64].
- : La Commission nationale de pharmacovigilance de l'Afssaps conclut qu'il n'est pas possible de laisser les patients face à un tel risque.
- : Malgré les alertes, une autorisation de mise sur le marché (AMM) est délivrée pour deux génériques du Mediator aux laboratoires Mylan et Qualimed[64].
- : Une étude effectuée par la Caisse nationale d'assurance maladie à partir de sa base de données d'une cohorte d'un million de diabétiques montre que le risque de chirurgie valvulaire est multiplié par près de quatre pour les patients exposés au Mediator.
- : La Commission Nationale de Pharmacovigilance de l'Afssaps note « un signal relatif aux anomalies des valvules cardiaques soupçonné depuis plusieurs mois par les données de pharmacovigilance ». À la fin de la réunion, la Commission ne rend pas d'avis[64].
- : L'autorisation de mise sur le marché (AMM) du benfluorex (Mediator et ses génériques) est suspendue[64].
- : L’Afssaps décide de suspendre le Mediator[65], ainsi que les deux génériques du Mediator qui venaient d'obtenir une Autorisation de Mise sur le Marché le . Selon l'Agence, un seul cas confirmé de valvulopathie cardiaque associée au Mediator a été déclaré jusqu’à la fin 2008.
- : Le benfluorex (Mediator et ses génériques) est retiré des pharmacies[64].
2010
modifier- : Irène Frachon publie son étude relative à l'association entre valvulopathie et prise de benfluorex[66].
- : Le groupe Servier publie dans le Quotidien du médecin et le Quotidien du pharmacien un communiqué déclarant : « Face aux nombreuses inexactitudes parues dans la presse grand public, à ce jour, aucun lien de causalité direct n'a été démontré entre la prise du médicament et les valvulopathies »[44].
- : Irène Frachon publie le livre Mediator 150 mg, combien de morts ? (éditions-dialogues.fr, 150 p.) qui raconte son histoire. L'éditeur est attaqué en justice par le laboratoire Servier[67]. Le sous-titre « Combien de morts? » est censuré [2].
- : La décision définitive d'interdiction par l'Agence européenne est prise, avec cet avis : « Le lien entre benfluorex et valvulopathie est établi[44] ».
- : Une thèse soutenue par Flore Michelet, docteur en pharmacie de l'université de Rennes I, intitulée Utilisation de nouveaux outils en pharmacovigilance : à propos du retrait du Mediator (benfluorex), relève que 300 000 personnes ont été chaque année exposées au Mediator[44]. Selon cet auteur, « il semblerait qu'il y ait eu ces dernières années entre 150 et 250 hospitalisations chaque année en France liées directement à une toxicité du Mediator, ayant entraîné une trentaine de décès. Si nous multiplions par 30 ans de commercialisation, le nombre de morts pourrait être entre 500 et 1 000 »[68]
- : Article du Figaro donnant les grandes tendances de l'étude de la CNAM, sous couvert de la Protection des sources d'information.
- : Publication dans la revue Pharmacoepidemiology and Drug Safety de l'étude de la CNAM montrant que le Mediator multipliait par 3 le risque de valvulopathie et par 4 le risque de chirurgie valvulaire[69],[70].
- : Selon une réunion de la Commission nationale de pharmacovigilance, une analyse de données de la CNAM-TS faite par l’épidémiologiste Catherine Hill (qui dirige le service d'épidémiologie des cancers de l'Institut Gustave-Roussy à Villejuif) confirme les premiers travaux qu’avait révélés Le Figaro en [71]. Selon ces études, le benfluorex (Mediator) serait bien responsable de 500 à 1 000 morts en France[68]. Le laboratoire Servier estime de son côté que ces chiffres sont des « hypothèses fondées sur des extrapolations ».
- : L’Afssaps estime à 500 le nombre de morts imputés au Mediator. 3 500 personnes ont été hospitalisées. 80 % des complications se produisent dans les deux années qui suivent l'arrêt du traitement. Elle annonce une série de mesures, en particulier une campagne d’information pour rechercher tous les patients qui ont pu prendre ce produit. Elle recommande aux personnes qui ont pris du Mediator pendant plus de trois mois de consulter leur médecin traitant[72].
- : Selon Jacques Servier, l'affaire du Mediator est une « fabrication »[73].
- : Dans une lettre adressée aux médecins français, Denys Schutz, médecin, directeur général de Servier-Biopharma écrit : « Les principes actifs de Mediator et d'Isoméride sont différents, tant en termes de structures chimiques que d'effets biologiques (…) ou en termes de métabolisme[53]. »
- : Martine Aubry, Bernard Kouchner et Martin Hirsch affirment n'avoir jamais été alertés[74],[75]. Xavier Bertrand affirme avoir pris connaissance de la dangerosité du Mediator en [76].
2011
modifier- À la suite d'un rapport[5] accablant de l'IGAS sur le Mediator[77], Xavier Bertrand lance une réforme du système français de pharmacovigilance[78].
- : Le professeur Acar, dans ses conclusions à propos des débats ouverts sur le sujet de la mortalité attribuable au benfluorex, indique : « Travail intéressant mais préliminaire dont il ne faut pas méconnaître les difficultés de réalisation. Il apporte des données utiles mais comporte des lacunes et des erreurs tenant à la méthodologie utilisée et à une analyse peu rigoureuse de la cohorte des patients décédés. Ces enquêtes ne permettent pas une estimation fiable de la fréquence des valvulopathies sévères liées au benfluorex. De ce fait, toute extrapolation sur ces bases à l'ensemble des patients exposés au benfluorex nous paraît arbitraire. Il serait souhaitable que d'autres enquêtes soient entreprises avec une méthodologie différente et une recherche rigoureuse des critères d'imputabilité de la complication cardiaque à telle ou telle étiologie[79]. »
- Parution en avril d'un article[80] estimant au minimum à 500 la mortalité attribuable au benfluorex (Mediator). L'article résume les données démontrant la toxicité cardiaque du médicament et explique la méthode utilisée pour l'estimation.
- : Parution du Rapport d'information No 675 de Mme Marie-Thérèse Hermange, fait au nom de la Mission commune d'information "Mediator : Évaluation et contrôle des médicaments"[81]. On apprendra en que ce rapport avait été modifié à l'avantage de Servier après une intervention de Claude Griscelli, un expert médical présenté comme proche du directeur opérationnel du groupe Servier, Jean-Philippe Seta[82]. C'est Mme Hermange qui a invité M. Griscelli à relire le rapport dans les locaux du Sénat : la sénatrice et l'expert proche de Servier sont donc mis en examen. Depuis, Jean-Philippe Seta a quitté l'entreprise Servier[83] et Mme Hermange a été nommée au comité d'éthique de l’Académie de médecine[84].
- : Deux anciens chercheurs des Laboratoires Servier, Jean Charpentier et Jacques Duhault, déclarent aux juges que les caractéristiques anorexigènes du Mediator (du fait de sa nature amphétaminique) ont été cachées pour en faire un antidiabétique, afin de faciliter l'obtention de son autorisation de mise sur le marché (AMM)[34].
2012
modifierEn 2012 paraissent les résultats d'un essai financé par les laboratoires Servier parmi une population de diabétiques recevant déjà tous un traitement antidiabétique et traités en plus, après tirage au sort, pendant un an, soit par benfluorex soit par pioglitazone[85]. Les patients devaient avoir une échographie cardiaque initiale puis au bout d'un an de traitement. L'essai montre qu'après un an de traitement, le risque d'apparition ou d'aggravation de valvulopathies est très supérieur dans le groupe benfluorex comparé à l'autre groupe (82/304 patients versus 33/300). Le risque d'atteinte de plusieurs valves est aussi très augmenté (16/304 versus 1/300).
2014
modifier- : 8 350 dossiers ont été déposés à l'ONIAM. 293 d'entre eux ont reçu un avis positif d'indemnisation. Pour Erik Rance, directeur de l’ONIAM, « ce faible taux d’avis positifs tient au fait que beaucoup de dossiers reçus ne concernaient pas les deux pathologies pour lesquelles la responsabilité des laboratoires Servier est reconnue : les valvulopathies et l’hypertension artérielle pulmonaire (HTAP)[24]. » Le collège évalue le « pourcentage du préjudice fonctionnel » et transmet le dossier aux laboratoires Servier. C'est le laboratoire qui fait ensuite une proposition chiffrée à la victime. Si cette proposition est jugée insuffisante, la victime peut saisir l’ONIAM qui, s’il le juge nécessaire, l’indemnise directement et se retourne ensuite contre le laboratoire pour obtenir remboursement. Douze victimes, jugeant l’offre de Servier insuffisante, se sont retournées vers l’ONIAM. « Nous n’avons pas donné suite, » indique Erik Rance, « car nous avons estimé que l’offre de Servier était convenable. »
Face aux critiques relatives au faible nombre d’avis positifs rendus, l’ONIAM indique que l'imputabilité du Mediator dans la survenue des pathologies précitées devait être établie « sur la base d’un lien direct et certain ». Cependant, le nombre de dossiers où l'imputabilité est reconnue devrait croître, depuis un arrêt de la Cour de cassation du selon lequel cette imputabilité peut s’établir « sur la base de présomptions graves, précises et concordantes »[24].
2016
modifierPlus de 6 000 dossiers ont été déposés auprès de l'ONIAM. Mais les patients doivent encore renverser la présomption de fraude. Selon Irène Frachon, « Les experts partent du principe que toute victime qui réclame une indemnisation est une fraudeuse[86]. »
Le , le Conseil d’État confirme l’analyse de la cour administrative d'appel de Paris, « qui a jugé que ce n’est qu’à partir de 1999 que l’État a commis une faute en ne prenant pas de mesures de suspension ou de retrait de l’autorisation de mise sur le marché du Mediator »[87].
2021
modifierL'affaire du Mediator se conclut en par un procès qui condamne Servier et l'Agence du médicament, à des amendes, à des peines de prison avec sursis et à indemniser les victimes.
2023
modifierServier est condamné en appel pour à une amende de près de 9 millions d'euros pour tromperie aggravée auprès des victimes du Mediator, mais également à une seconde amende de 415 millions d'euros pour délit d'escroquerie, alors que le laboratoire avait été relaxé de ce délit en première instance[88],[89].
Présentation - Posologie
modifier- Comprimé enrobé (blanc) : boîte de 30.
- Composition :
- benfluorex chlorhydrate, 150 mg par comprimé ;
- excipients.
- Posologie : 3 comprimés par jour[90].
Données cliniques
modifierIndications thérapeutiques
modifierAvant son retrait le , le benfluorex est indiqué dans le traitement du diabète de type 2 ou diabète non insulinodépendant. Il est aussi prescrit aux personnes désireuses de perdre du poids.
Contre-indications
modifier- Hypersensibilité au chlorhydrate de benfluorex ou à l'un des constituants.
- Pancréatites chroniques avérées.
Propriétés pharmacologiques
modifierSelon l'IGAS, le laboratoire a trompé les autorités sanitaires. Le benfluorex n'a aucune activité pharmacologique propre ; il est le précurseur d'une molécule active (et toxique), la norfenfluramine, proche de l'amphétamine. Selon le rapport de l'IGAS, « Cet « aveu » de ce que le benfluorex ne serait qu’un précurseur, c’est-à-dire une molécule n’ayant en elle-même aucune activité pharmacologique, les laboratoires Servier ont cherché, après l’avoir reconnu, à le faire oublier, en retirant une phrase évoquant cette caractéristique d’un document communiqué à l’Afssaps en 1999[5] » (en gras dans le texte).
Propriétés pharmacodynamiques
modifierLe benfluorex (Mediator) et l'Isoméride agissent tous deux par l'intermédiaire d'un métabolite identique, la norfenfluramine[91] ; ils ont donc des caractéristiques pharmacologiques très proches. Les deux produits ont une efficacité hypoglycémiante prouvée en double insu contre placebo, mais cette efficacité est moindre que celle des antidiabétiques de référence comme la metformine[92].
- Propriétés mises en avant dans la documentation officielle :
- hypolipidémiant ;
- hypocholestérolémiant ;
- hypoglycémiant.
- Propriété absente de la documentation officielle :
- anorexigène, en commun avec l'Isoméride[93].
C'est cette activité anorexigène, ou coupe-faim (non officielle puisque l'indication validée par l'Agence du médicament est : « certaines formes de diabète »), qui a été mise en avant auprès des prescripteurs par les visiteurs médicaux de Servier, ce qui explique la répartition géographique des ventes : selon les données de la CNAM, le Mediator atteignait des records de consommation sur la côte méditerranéenne[94].
Le métabolite toxique pour les valves cardiaques produit par ces deux médicaments est la norfenfluramine. La norfenfluramine n'est pas présente dans les comprimés d'Isoméride ou de Mediator : elle est produite par la modification de ces médicaments - ou métabolisme - dans l'organisme. Dans une large mesure, le benfluorex (Mediator) est une prodrogue de la norfenfluramine.
Le niveau d'exposition à la norfenfluramine est similaire, que l'on prenne du Mediator ou de l'Isoméride[50], mais variable d'une personne à l'autre. On ne connaît pas les facteurs associés à cette variabilité.
Propriétés pharmacocinétiques et métabolisation
modifierLe benfluorex est complètement métabolisé. Il ne circule dans le plasma sanguin qu’à des taux indétectables, car « immédiatement transformé en son métabolite S422, puis en métabolite S1475 et en norfenfluramine (S585) », qui est un puissant anorexigène[5]. Le benfluorex est une prodrogue, un ester benzoïque qui, rapidement hydrolysé, donne l'alcool S422, lequel s'oxyde pour donner l'acide S1475 ; ces deux dérivés ont une durée de vie très courte et laissent rapidement place à la norfenfluramine (S585)[95],[96].
Interdiction
modifierMis sur le marché en France en 1976, le Mediator sera retiré du marché belge en 1978, du marché suisse en 1997 et espagnol en 2003. En France, le Mediator a échappé à l'interdiction de 1997[97]. Lors de son retrait en France à la fin [98], environ 200 000 patients étaient encore traités par le benfluorex.
Procédures administratives et judiciaires
modifierDe nombreuses procédures judiciaires sont engagées par des personnes s'estimant victimes du produit et mal informées des risques d'hypertension artérielle pulmonaire et de valvulopathie cardiaque.
Jacques Servier
modifierDans un livre intitulé Le Médicament : inventer ou mourir, publié aux éditions de La Table Ronde en 1982, Jacques Servier présentait son point de vue sur l'industrie du médicament, plaidant pour une plus grande liberté pour les industriels de la pharmacie et regrettant les contrôles trop coûteux, « étouffants » pour la créativité, ainsi qu'une tendance à l'« alourdissement des contrôles ». Il y estimait que « le plus désastreux chez nous est la multiplicité des initiatives des pouvoirs publics. Tant d'instances accumulent les réglementations qu'elles réussissent à créer une atmosphère de harcèlement administratif incompatible avec la vie » et considérait que « c'est le bon sens des dirigeants de l'industrie pharmaceutique, coloré d'une véritable obsession d'éviter toute possibilité d'accident. Jamais les médicaments n'en sortent [des laboratoires] avant que des animaux en aient absorbé des échantillons[99]. »
Dans les années 1990, les laboratoires Servier dominaient le marché des coupe-faim, médicaments augmentant la sensation de satiété, en particulier à l'égard des sucres, et sans les effets excitants et toxicomanogènes des produits plus anciens, avec deux produits : l’Isoméride puis le Mediator. L'Isoméride, soupçonné de favoriser l’hypertension artérielle pulmonaire (HTAP), est retiré du marché en 1997. À la même époque, le directeur scientifique de Servier est le trésorier de la Société française de pharmacovigilance et de thérapeutique[52].
À nouveau, début 2011, Pierre Schiavi, directeur de la division scientifique « pharmacologie et gériatrie » chez Servier, était aussi trésorier de la Société française de pharmacologie et de thérapeutique[100].
Jacques Servier, président et fondateur du laboratoire portant son nom, a été fait grand-croix de la Légion d'honneur par le président Sarkozy, le . Ce dernier a précédemment été un des avocats du groupe Servier[101].
À propos des décès imputables au Mediator, Jacques Servier déclarait, début 2011 :
« Cinq cents est un très beau chiffre marketing, mais il ne s'agit que de trois morts[102]. »
Jacques Servier, qui devait comparaître pour tromperie aggravée lors d'un procès au pénal renvoyé à 2015, est mort le . L'action publique à son encontre est donc éteinte, mais son décès ne met pas un terme aux procédures engagées contre le groupe[103].
Notes et références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- "International Symposium on Amphetamines and Related Compounds, Proceedings, Mario Negri Institute for Pharmacological Research, Milan, 1969," Costa, E., and S. Garattini, eds., New York, Raven Press, 1970Vol. -, Pg. 21, 1970
- "International Symposium on Amphetamines and Related Compounds, Proceedings, Mario Negri Institute for Pharmacological Research, Milan, 1969," Costa, E., and S. Garattini, eds., New York, Raven Press, 1970Vol. -, Pg. 21, 1970.
- (en) « Benfluorex », sur ChemIDplus, consulté le 16/11/2010
- Rapport et annexes sur le Mediator, par l'IGAS, commandé par le ministre du Travail de l’emploi et de la santé et la secrétaire d'État chargée de la Santé, pour mettre en lumière la succession des évènements et des choix portant sur ce médicament afin de comprendre les mécanismes de prises de décision.
- Il était aussi présent dans les génériques Benfluorex 150 mg des laboratoires Mylan et Benfluorex 150 mg de Qualimed.
- « Mediator : Ce poison a permis à Servier de gagner 1 milliard d'euros », Le Point, 22 septembre 2019.
- L'article fenfluramine donne des indications sur la chronologie du retrait des fenfluramines dans plusieurs pays vers la fin de l'année 1997.
- Frank Browning et John Gerassi, Histoire criminelle des États-Unis, Nouveau monde, , p. 8.
- « Mediator: la responsabilité civile de Servier validée », Le Figaro, 22 septembre 2017.
- « Mediator : la responsabilité des Laboratoires Servier est scellée », Dalloz actualité, .
- « Le Mediator serait responsable de 500 à 1 000 morts en France », Le Monde, 13 octobre 2010.
- Nathalie Courret, « Mediator hors AMM : quelle est la responsabilité des médecins ? », sur santemagazine.fr, Santé Magazine, .
- « Laboratoires Servier, anatomie d’un système », Libération, (lire en ligne)
- lefigaro.fr, « Mediator, le scandale sanitaire », sur lefigaro.fr (consulté le ).
- « Le scandale du Mediator et Jacques Servier », LExpress.fr, (lire en ligne, consulté le ).
- « Scandale du Mediator : la responsabilité civile de Servier rejugée en appel », Le Monde.fr, (ISSN 1950-6244, lire en ligne, consulté le ).
- Étude Ings & Gordon, 1990, citée p. 6 du rapport d'étude Servier The pharmacokinetics of the metabolites of benfluorex… 1993.
- « Mediator: Bertrand recommande à tous les patients de consulter », dépêche Agence France-Presse.
- Voir sur lefigaro.fr.
- Voir sur Le Monde.fr du 9 février 2012.
- « Estimate of deaths due to valvular insufficiency attributable to the use of benfluorex in France ».
- Le Médiator® Informations pour les patients.
- « Mediator : 8350 dossiers déposés à l'ONIAM, 293 avis positifs d'indemnisation » Le Quotidien du médecin, 23 janvier 2014.
- US 3,607,909
- brevet français FR 6564M
- Pourquoi l'affaire du Mediator a-t-elle mis si longtemps à éclater ?, Le Monde, 23 novembre 2010
- Chronique OMS volume 25, no 3 de mars 1971
- OMS, The use of common stems in the selection of International Nonproprietary Names (INN) for pharmaceutical substances, Genève, 2002, p. 89-90
- International Nonproprietary Names, OMS
- J. M. Kay, Paul Smith, Donald Heath, « Aminorex and the Pulmonary Circulation », Thorax, vol. 26, no 3, , p. 262-270 (ISSN 1468-3296, PMID 5089490, DOI 10.1136/thx.26.3.262, lire en ligne, consulté le )
- Mediator : l'enfant "caché" de l'amphétamine, Science et Avenir, 18 janvier 2011
- Philippe Lechat (2010), « Propriétés pharmacologiques du benfluorex ».
- « Le laboratoire Servier mis en cause pour un autre médicament, le Protelos » Le Monde, 7 septembre 2011.
- Article du site Marianne, « Mediator : critiqué en 1976, dès sa mise sur le marché ».
- Voir sur tempsreel.nouvelobs.com.
- « Dès 1977, les Belges refusent de commercialiser le Mediator » Le Figaro, 31 janvier 2011.
- J.G Douglas et coll, Pulmonary hypertension and fenfluramine, British Medical Journal, octobre 1981
- Voir sur ncbi.nlm.nih.gov.
- Voir sur sciencedirect.com.
- Voir sur sciencedirect.com.
- B.H. Gordon (1993) The pharmacokinetics of the metabolites of benfluorex in chronic administration [… in human volunteers Servier Report No. 93-5792-001]
- [1] F. Brenot et coll, Primary pulmonary hypertension and fenfluramine use, British Heart Journal, décembre 1993
- Mediator : Combien de morts ?, Le Monde, 24 août 2010
- Mediator : la schizophrénie de l'Agence du médicament lefigaro.fr 25/01/2011
- L. Abenhaïm et coll, Appetite-suppressant drugs and the risk of primary pulmonary hypertension, New England Journal of Medecine, 29 août 1996
- Le Mediator interdit en Suisse dès 1997, Le Monde, 21 janvier 2011
- Mediator : le conseil de l'ordre sanctionnait les surprescriptions, Le Monde, 18 décembre 2010
- Mediator : l'agence du Médicament inquiète dès 1998, Le Figaro, 1 janvier 2010
- Mediator: l'Assurance maladie mettait en garde dès 1998, Le Figaro, 17 décembre 2010
- « Précisions de l'ancien directeur général de l'Agence du médicament », Le Figaro, 11 janvier 2011
- Mediator, coupe-faim dangereux et longtemps toléré, Libération, 16 novembre 2010
- « Des experts avaient alerté des dangers du Mediator dès 1999 », Le Figaro, (lire en ligne)
- [PDF] « Possible Role of Valvular Serotonin 5-HT2B Receptors in the Cardiopathy Associated with Fenfluramine ».
- (en) Rothman et al. « Evidence for possible involvement of 5-HT2B receptors in cardiac valvulopathy associated with fenfluramine and other serotonergic medications » Circulation, décembre 2000
- (en) Rafel Ribera J, Casañas Muñoz R, Anguera Ferrando N, Batalla Sahún N, Castro Cels A, Pujadas Capmany R, « Valvular heart disease associated with benfluorex », Rev Esp Cardiol, vol. 56, no 2, , p. 215–216 (PMID 12605770, lire en ligne)
- « En 2003, l'Espagne retire le Mediator du marché », Le figaro santé, (lire en ligne, consulté le )
- « 200 médicaments passés au crible », Science & Vie, , p. 86
- CNPV du 29 novembre 2005, afssaps.fr
- « Il faudrait un Prescrire pour le grand public ! », sur arretsurimages.net, (consulté le )
- « En Espagne, la survenue sous benfluorex de troubles cardiaques graves, semblables à ceux observés avec la fenfluramine et la dexfenfluramine, est à l'origine du retrait du marché des spécialités pharmaceutiques contenant du benfluorex, en mars 2003. La revue Prescrire estime que les autorités françaises seraient bien avisées de suivre l'exemple de l'Espagne. » La revue Prescrire, 1er septembre 2005
- « Deux anciens conseillers de Xavier Bertrand étaient payés par le laboratoire Servier », sur France 24, (consulté le )
- Canard enchaîné, 12 janvier 2011
- octobre 2009: Quand l'Afssaps autorisait les génériques du Mediator…, Le Figaro, 20 décembre 2010
- Décision de l'AFSSAPS
- Irène Frachon et coll., Benfluorex and Unexplained Valvular Heart Disease : A Case-Control Study, PLOS One, avril 2010. DOI 10.1371/journal.pone.0010128
- Le livre Mediator, combien de morts ? attaqué en justice. Décision le 7 juin, Le Télégramme, 1er juin 2010
- Comment s'est construite l'estimation de 500 morts dues à la prise du Mediator, Le Monde, 30 novembre 2010
- Alain Weill, Michel Païta, Philippe Tuppin, Jean-Paul Fagot, Anke Neumann, Dominique Simon, Philippe Ricordeau, Jean-Louis Montastruc and Hubert Allemand, Benfluorex and valvular heart disease: a cohort study of a million people with diabetes mellitus., Pharmacoepidemiology and drug safety (2010)
- Mediator : une deuxième étude confirme le risque, Le Figaro, 15 octobre 2010
- Le Mediator serait responsable de 500 à 1 000 décès en France, Le Figaro, 13 octobre 2010
- Le Mediator aurait fait 500 morts en 30 ans, selon l'Afssaps, Le Monde, 16 novembre 2010
- L'affaire du Mediator®, une « fabrication » selon Servier, Le Figaro, 21 novembre 20100
- Voir sur lejdd.fr.
- Voir sur lexpress.fr.
- Voir sur lefigaro.fr.
- « Médicament : des mesures urgentes pour restaurer la confiance » (Impact Médecine no 347 p. 4-5 - 20/1/2011) notice 1856.
- « La pharmacovigilance va faire peau neuve : du passé, table rase » Le Quotidien du Médecin, no 8885, p. 4, 14 janvier 2011.
- Acar J., « Benfluorex, valvulopathies et décès : un autre regard ».
- Hill C. « Mortalité attribuable au benfluorex (Mediator) » La Presse Médicale, 2011, vol. 40, p. 462-469. DOI 10.1016/j.lpm.2011.03.001, article.
- Sénat : Rapport d'information no 675 - 28 juin 2011
- Mediator : comment Servier a corrigé le rapport du Sénat lefigaro.fr
- Jacques Servier évince son numéro deux - lemonde.fr
- Mediator: l’Académie maintient la sénatrice mise en examen - lefigaro 27 février 2017
- (en) Derumeaux G, Ernande L, Serusclat A, Servan E, Bruckert E. et al. « Echocardiographic Evidence for Valvular Toxicity of Benfluorex: A Double-Blind Randomised Trial in Patients with Type 2 Diabetes Mellitus » PLOS One, 2012, vol. 7(6): e38273. DOI 10.1371/journal.pone.0038273
- Libération, 20 mai 2016
- « Responsabilité de l'État dans l'affaire du Mediator », sur conseil-etat.fr, .
- « Affaire du Mediator : le groupe Servier condamné en appel pour escroquerie à rembourser plus de 415 millions d'euros à l'assurance-maladie et aux mutuelles », sur Franceinfo, (consulté le )
- « Procès du Mediator : Servier condamné en appel à rembourser plus de 415 millions aux organismes de Sécurité sociale », Le Monde, (lire en ligne, consulté le )
- VIDAL 1997, Paris.
- ou son énantiomère S, pour l'Isoméride
- MEDIATOR-BIAM
- ISOMERIDE-BIAM
- Mediator: l'étrange effet Méditerranée (mediapart)
- « MEDIATOR : Reconnu dangereux dès 1995, selon le rapport de l'IGAS », Santé log, (lire en ligne)
- « Propriétés pharmacologiques du benfluorex - Dr. Philippe Lechat, Afssaps » [PDF], sur ANSM (consulté le )
- Médiator: début d’un procès hors norme, 22 septembre 2019
- Diabète : 3 médicaments retirés, Le Figaro, 26 novembre 2009
- « Mediator : un médecin guînois exhume un vieux livre de Jacques Servier » sur lavoixdunord.fr, lundi 18 avril 2011.
- Sénat - Mission commune d'information sur le Mediator.
- « Mediator, la fin du coupe-faim », Libération, 1er juin 2010.
- « Mediator : Bertrand “stupéfait” par les propos de Servier », Le Parisien, 6 janvier 2011.
- « Jacques Servier, fondateur des laboratoires du même nom, est mort », lefigaro.fr, 16 avril 2014.]
Voir aussi
modifierBibliographie
modifier- C. Lalo, P. Solal, Le Livre noir du médicament, Plon, (ISBN 9782259215855) ; présentation sur plon.fr
- « Utilisation de nouveaux outils en pharmacovigilance : À propos du retrait du Mediator® (benfluorex) », thèse pour le diplôme d'État de docteur en pharmacie, Flore Michelet sous la direction du Pr G. Le Gal,
Filmographie
modifier- La Fille de Brest (2016) d'Emmanuelle Bercot Retrace le combat de la pneumologue Irène Frachon pour faire connaître les risques associés à l'utilisation du Mediator ; voir « La Fille de Brest (2017) sur cinoche.com » (consulté le ).