Annulène
Les annulènes sont des hydrocarbures cycliques complètement conjugués. Ils sont pour formule générale CnHn pour n un entier naturel pair, ou CnHn+1 si n est impair. Les conventions IUPAC[1] sont que les annulènes avec 7 ou plus atomes de carbone sont nommés [n]annulène, où n est le nombre d'atomes de carbone dans leur cycle. Cependant, souvent, les annulènes plus petits (n<7) sont référencés sous la même convention et le benzène, lui-même, appelé simplement annulène[2],[3].



Les trois premiers annulènes pairs sont le cyclobutadiène, le benzène et le cyclooctatétraène (COT ou [8]annulène).
Les annulènes peuvent être :
- aromatiques comme le benzène, le [14]annulène (en), le cyclooctadécanonaène ou [18]annulène.
- non-aromatique comme le COT.
- antiaromatique comme le cyclobutadiène, le cyclodécapentaène (en) ou le [10]annulène[4] et le cyclododécahexaène (en) ou [12]annulène, ces composés étant généralement instables.
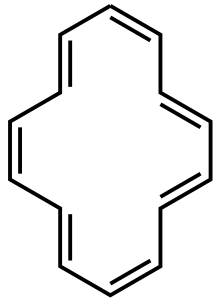
Seuls le cyclobutadiène et le benzène sont parfaitement plats. Cependant le [14]annulène avec une double liaison sur 2 en position E (trans) et le [18]annulène avec une double liaison sur 3 en position E - ce qui place dans les deux cas, des atomes d'hydrogène à l'intérieur du cycle- peuvent avoir une conformation plane nécessaire pour l'aromaticité, ces deux composés suivant la règle de Hückel avec 4n+2 électrons π. Le [14]annulène a un cycle contraint du fait de l'encombrement stérique qui le rend instable.
Beaucoup des annulènes les plus grands, comme le [18]annulène, sont suffisamment larges pour minimiser l'encombrement stérique de leurs hydrogènes internes et sont qualifiés de thermodynamiquement aromatiques. Cependant aucun de ces grands annulènes n'est autant stabilisé que le benzène et leur réactivité ressemble plus à celle de polyènes conjugués qu'à celle des hydrocarbures aromatiques.
Dans les annulynes, une double liaison est remplacée par une triple liaison, caractéristique des alcynes.
Notes
modifier- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Annulene » (voir la liste des auteurs).
- (en) « annulenes », IUPAC, Compendium of Chemical Terminology [« Gold Book »], Oxford, Blackwell Scientific Publications, 1997, version corrigée en ligne : (2019-), 2e éd. (ISBN 0-9678550-9-8)
- Ege, S. (1994) Organic Chemistry:Structure and Reactivity, 3rd ed., D.C. Heath and Company
- Dublin City University : Annulènes
- l'aromaticité du [10]annulène est parfois débattue car certains isomères semblent être suffisamment plans pour respecter la règle de Hückel, voir (en) [1] mais aussi (en) [2]