Chlorure d'américium(III)
composé chimique
(Redirigé depuis AmCl3)
Le chlorure d'américium(III) ou trichlorure d'américium est le composé chimique constitué d'américium et de chlore de formule AmCl3. Il forme des cristaux roses hexagonaux.
| Chlorure d'américium(III) | |
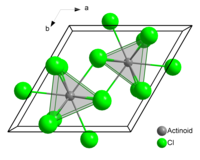
| |
| Structure du chlorure d'américium(III) : __ Am3+ __ Cl− | |
| Identification | |
|---|---|
| No CAS | |
| SMILES | |
| InChI | |
| Apparence | cristaux roses opaques |
| Propriétés chimiques | |
| Formule | AmCl3 [Isomères] |
| Masse molaire[1] | 349 g/mol Am 69,65 %, Cl 30,48 %, |
| Propriétés physiques | |
| T° fusion | 715 °C[2] |
| T° ébullition | 850 °C[3] |
| Masse volumique | 5,87 g·cm-3[3] |
| Cristallographie | |
| Système cristallin | Hexagonal |
| Symbole de Pearson | |
| Classe cristalline ou groupe d’espace | (no 176) |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
À l'état solide, chaque atome d'américium a neuf atomes de chlore comme proches voisins, approximativement à la même distance[4],[5].
L'hexahydrate a une structure cristalline monoclinique avec : a = 970,2 pm, b = 656,7 pm et c = 800,9 pm ; β = 93° 37' ; groupe d'espace : P2/n[6].
Réactions
modifierUne méthode d'électroraffinage (en) utilisant du chlorure d'américium(III) a été étudiée pour le séparer des mélanges d'actinides, puisque l'énergie libre de Gibbs standard de formation du chlorure d'américium(III) est très différente des autres chlorures d'actinides[7].
Notes et références
modifier- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Americium(III) chloride » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Dale L. Perry et Sidney L. Phillips, Handbook of Inorganic Compounds, Boca Raton/New York/London (etc.), CRC Press, (ISBN 0-8493-8671-3, lire en ligne), p. 15
- « Chemistry: Periodic Table: americium: compound data (americium (III) chloride) », WebElements (consulté le )
- (en) L. B. Asprey, T. K. Keenan et F. H. Kruse, « Crystal Structures of the Trifluorides, Trichlorides, Tribromides, and Triiodides of Americium and Curium », Inorg. Chem., vol. 4, no 7, , p. 985–986 (DOI 10.1021/ic50029a013).
- (en) A. F. Wells, Structural Inorganic Chemistry, Oxford, Oxford Science Publications, , 5e éd., 1382 p. (ISBN 0-19-855370-6).
- (en) John H. Burns et Joseph Richard Peterson, « The Crystal Structures of Americium Trichloride Hexahydrate and Berkelium Trichloride Hexahydrate », Inorg. Chem., vol. 10, no 1, , p. 147–151 (DOI 10.1021/ic50095a029).
- (en) Nuclear Energy Agency, Proceedings of the Workshop on Pyrochemical Separations, Avignon, France, OECD Publishing, , 336 p. (ISBN 92-64-18443-0, lire en ligne).


