Xylitol
Le xylitol (E967) est un polyol extrait de l'écorce de bouleau, considéré depuis une vingtaine d'années comme un substitut du sucre classique (saccharose) dans les pays nordiques. Le xylitol est communément appelé sucre de bouleau.
| Xylitol | |
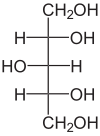
| |
| Identification | |
|---|---|
| Nom UICPA | (2R,3R,4S)-pentane- 1,2,3,4,5-pentanol |
| Synonymes |
1,2,3,4,5-Pentahydroxypentane |
| No CAS | |
| No ECHA | 100.001.626 |
| No CE | 201-788-0 |
| PubChem | |
| No E | E967 |
| Apparence | Solide modérément hygroscopique |
| Propriétés chimiques | |
| Formule | C5H12O5 [Isomères] |
| Masse molaire[1] | 152,145 8 ± 0,006 3 g/mol C 39,47 %, H 7,95 %, O 52,58 %, |
| Propriétés physiques | |
| T° fusion | 93,5 °C[2] |
| T° ébullition | 216 °C[2] |
| Solubilité | 1 dans 80 parts (éthanol, 20 °C), très peu sol. dans la glycérine, |
| Masse volumique | 1,52 g·cm-3 [3] |
| Écotoxicologie | |
| DL50 | ≈22 g·kg-1 (souris, oral) |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Certains avantages comme ses effets antibactériens en font une réponse possible aux problèmes de santé publique liés à la surconsommation de sucre, ou comme solution de traitement de la sinusite[4].
Goût
modifierLe xylitol possède le même pouvoir sucrant et la même saveur que le saccharose (pouvoir sucrant quasi similaire). En revanche, le xylitol a un effet rafraîchissant et son apport calorique est inférieur à celui du saccharose avec 2,4 kcal/g contre 4,0 kcal/g.
Le xylitol, comme la plupart des polyols tels l'érythritol, le mannitol et le sorbitol, produit un effet rafraîchissant en bouche. Cependant, il est celui qui produit l'effet le plus prononcé parmi les polyols. Pour cette raison, le xylitol est l'édulcorant de friandises « rafraîchissant l'haleine ».
De plus, le xylitol a un indice glycémique très faible qui en fait un atout dans la lutte contre les crises d'hyperglycémie (indice glycémique de 7).
Chimie
modifierLe xylitol est un polyol (sucre alcool). La formule brute du xylitol est C5H12O5. Son nom systémique est (2,3,4,5)tetrahydroxy-pentanol mais peut être dénommé dans différents ouvrages comme : 1,2,3,4,5-Pentahydroxypentane D-Xylit ou (2R,3R,4S)-pentane-1,2,3,4,5-pentanol.
Il fut découvert et synthétisé en 1891 par Hermann Emil Fischer, chimiste allemand, et ses associés[5]. Le xylitol est dangereux pour les chiens[6].
Occurrences
modifierOccurrence du xylitol en mg/100g de matière sèche :
| aliment | mg pour 100g de matière sèche[7] |
|---|---|
| bananes | 21 |
| framboises | 268 |
| fraises | 362 |
| chou-fleur | 300 |
| champignons de Paris | 128 |
Consommation
modifierLe xylitol est considéré comme à pouvoir cariogène nul. Préférable surtout dans les produits pastilles, les bonbons et les médicaments. Mais la consommation doit être réduite en raison de leur effet secondaire laxatif, à forte dose il peut être la cause d'une perte de réponse musculaire et nerveuse au niveau intestinal. Cependant, l'effet réducteur de caries de l'ajout de chewing-gum au xylitol à l'alimentation quotidienne a été bien démontré chez les enfants et les adolescents présentant un niveau de caries élevé ou modéré[9].
Effets secondaires
modifierSa consommation est corrélé avec une augmentation du risque de survenue d'une maladie cardiovasculaire. L'un des mécanismes possibles est l'augmentation de l'activité des plaquettes avec le risque de thrombose[10].
Chez le chien, il peut provoquer une hypoglycémie ainsi qu'une insuffisance hépatique aiguë[11].
Production
modifierLe xylitol est présent dans de nombreux fruits et baies mais son extraction commerciale à partir de ces sources n'est pas envisagée. Il est extrait du bois, des épis de maïs, de la pulpe de canne, des cosses de graines, de la paille, des coques de noix de coco. Ces sources contiennent 20-35 % de xylane qui est convertie en xylose par hydrolyse acide, puis hydrogénée (catalyse Ni ou chromite Cr) pour obtenir le xylitol (conversion du groupement —CHO terminal en —CH2OH)[3],[12]. L'hydrogénation est suivie de plusieurs étapes de séparation et de purification. Le produit final contient très peu d'impuretés, parmi lesquelles apparaissent le mannitol, le sorbitol, le galactitol ou l'arabitol.
Les autres méthodes de production plus rarement employées consistent en la conversion du glucose (dextrose) en xylose suivie d'une hydrogénation pour obtenir le xylitol, ou la conversion microbiologique du xylose en xylitol[3],[13].
Notes et références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Xylitol », sur ChemIDplus, consulté le 27 septembre 2009
- (en) Raymond C Rowe, Paul J Sheskey, Marian E Quinn, Handbook of Pharmaceutical Excipients, Londres, Pharmaceutical Press and American Pharmacists Association, , 6e éd., 888 p. (ISBN 978-0-85369-792-3), p. 786
- Joshua D. Weissman, Francisca Fernandez et Peter H. Hwang, « Xylitol nasal irrigation in the management of chronic rhinosinusitis: a pilot study », The Laryngoscope, vol. 121, no 11, , p. 2468–2472 (ISSN 1531-4995, PMID 21994147, DOI 10.1002/lary.22176, lire en ligne, consulté le )
- (en) Lyn O'Brien Nabors, Alternative sweeteners, New York, CRC Press, , 3e éd., 553 p. (ISBN 978-0-8247-0437-7, LCCN 2001028939, lire en ligne), p. 335-367
- (en) Jeffrey M. Todd et Lisa L. Powell, « Xylitol intoxication associated with fulminant hepatic failure in a dog », Journal of Veterinary Emergency and Critical Care, vol. 17, no 3, , p. 286–289 (ISSN 1476-4431, DOI 10.1111/j.1476-4431.2007.00243.x, lire en ligne, consulté le )
- (en) John M. deMan, Principles of food chemistry, Gaithersburg (Ma.), Aspen Publishers, , 3e éd., 595 p. (ISBN 0-8342-1234-X), p. 169
- (en) « Xylimax », sur Fazer.com (consulté le )
- K. Pienihäkkinen, A. Hietala-Lenkkeri, I. Arpalahti et E. Söderling, « The effect of xylitol chewing gums and candies on caries occurrence in children: a systematic review with special reference to caries level at study baseline », European Archives of Paediatric Dentistry: Official Journal of the European Academy of Paediatric Dentistry, (ISSN 1996-9805, PMID 38430364, DOI 10.1007/s40368-024-00875-w, lire en ligne, consulté le )
- Witkowski M, Nemet I, Li XS et al. Xylitol is prothrombotic and associated with cardiovascular risk, Europ Heart J, 2024;45:2439–2452,
- Murphy LA, Coleman AE, Xylitol toxicosis in dogs, Vet Clin North Am Small Anim Pract, 2012;42:307–12
- A. Etournaud, Chimie des denrées alimentaires pour laborantin(e)s en chimie et biologie, Laboratoire cantonal,
- http://www.artac.info/fic_bdd/pdf_fr_fichier/Classification_des_additifs_13299194710.pdf
Voir aussi
modifierArticles connexes
modifierLiens externes
modifier- Xylitol - Mâcher, c'est la santé ? Doctissimo
- Fiche technique du xylitol avec une description simplifiée du polyol
- (en) FAO monographe : Xylitol JECFA
- (en) http://www.preventivevet.com/xylitol-products-toxic-for-dogs