Sumatriptan
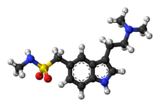
Le sumatriptan est un médicament de la classe des triptans, utilisé dans le traitement de la migraine et de l'algie vasculaire de la face. Sa structure est analogue à celle des alcaloïdes naturels comme la diméthyltryptamine, la bufoténine, et la 5-méthoxy-diméthyltryptamine, avec un groupe N-méthyl sulfonamidométhyle en position C5 sur le cycle indole. Le sumatriptan est produit par des laboratoires différents et il existe sous différents noms commerciaux : Imitrex, Treximet, ou Imigran.
| Sumatriptan | ||

| ||
 | ||
| Identification | ||
|---|---|---|
| No ECHA | 100.130.518 | |
| DrugBank | DB00669 | |
| PubChem | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | C14H21N3O2S [Isomères] |
|
| Masse molaire[1] | 295,4 ± 0,019 g/mol C 56,92 %, H 7,17 %, N 14,22 %, O 10,83 %, S 10,86 %, |
|
| Données pharmacocinétiques | ||
| Excrétion | ||
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
Mécanisme d'action
modifierLe sumatriptan a une structure apparentée à la sérotonine (5HT) et fait partie de la même classe (type 5-HT1D et 5-HT1B[2]). Les types de récepteurs qu'il active sont présents au niveau des vaisseaux du crâne. Il réduirait ainsi l'inflammation locale. L'activation de ces récepteurs entraine une vasoconstriction des artères dilatées au cours des crises migraineuses.
Le sumatriptan est également capable de diminuer l'activité du nerf trijumeau, ce qui expliquerait son rôle dans l'algie vasculaire de la face. Sous forme injectable, ce médicament a montré une efficacité dans le traitement des crises[3].
Pharmacocinétique
modifierLe sumatriptan est disponible sous plusieurs formes telles que les comprimés, l'injection sous-cutanée ou le spray nasal. Ce médicament est peu utilisé par voie orale du fait d'une biodisponibilité faible. En injection le sumatriptan agit rapidement (dans les dix minutes), et son effet dure moins longtemps. Le sumatriptan est métabolisé par la monoamine oxydase A en un analogue de l'acide indole 3-acétique. Ce métabolite est en partie conjugué à l'acide glucuronique, et excrété par voie urinaire et biliaire. Approximativement 3 % du principe actif original est éliminé avant d'être métabolisé.
Il n'existe pas de relation simple entre la concentration sanguine de la molécule et son effet antimigraineux. Ce paradoxe a été en quelque sorte résolu en comparant les différents taux d'absorption des différentes formes galéniques[4],[5].
Efficacité
modifierLors d'une migraine, l'injection sous cutanée de sumatriptan permet la résolution de la crise dans deux tiers des cas. Cette efficacité est moindre par voie orale[6]. L'association à du naproxène est synergique[7].
Ce type de médicament ne constitue pas un traitement de fond pour une migraine récidivante.
Effets secondaires
modifierÀ forte dose, le sumatriptan peut entraîner une sulfhémoglobinémie, une affection rare caractérisée par une coloration du sang vert foncé, en rapport avec l'intégration de soufre à l'hémoglobine des globules rouges[8]. L'arrêt du sumatriptan permet la guérison en quelques semaines.
Des effets secondaires cardiaques graves et parfois létaux, survenus après l'utilisation de sumatriptan, ont été rapportés. On peut citer un vasospasme coronarien, une ischémie myocardique transitoire un infarctus du myocarde, une tachycardie ventriculaire ou une fibrillation ventriculaire.
Les effets secondaires les plus fréquemment rapportés[9] dans les essais cliniques sur la migraine sont des sensations anormales (paresthésies, sensations de chaud/froid), des sensations d'oppression, des vertiges, des malaises et des troubles du sommeil.
Synthèse
modifierSynthèse monotope
modifierKnoll
modifierRéaction de Japp-Klingemann
modifierNotes et références
modifier- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « sumatriptan » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Razzaque Z, Heald MA, Pickard JD et al., « Vasoconstriction in human isolated middle meningeal arteries: determining the contribution of 5-HT1B- and 5-HT1F-receptor activation », Br. J. Clin. Pharmacol., vol. 47, no 1, , p. 75–82 (PMID 10073743, PMCID 2014192, DOI 10.1046/j.1365-2125.1999.00851.x)
- (en) Treatment of acute cluster headache with sumatriptan, The Sumatriptan Cluster Headache Study Group, N. Engl. J. Med., 1991;325:322-6.
- (en) A. W. Fox, « Onset of effect of 5-HT1B/1D agonists: a model with pharmacokinetic validation », Headache, vol. 44, no 2, , p. 142–147 (PMID 14756852, DOI 10.1111/j.1526-4610.2004.04030.x)
- (en) E. Freidank-Mueschenborn et A. Fox, « Resolution of concentration-response differences in onset of effect between subcutaneous and oral sumatriptan », Headache, vol. 45, no 6, , p. 632–637 (PMID 15953294, DOI 10.1111/j.1526-4610.2005.05129a.x)
- Derry CJ, Derry S, Moore RA, Sumatriptan (all routes of administration) for acute migraine attacks in adults—overview of Cochrane reviews, Cochrane Database Syst Rev, 2014; 5CD009108
- Law S, Derry S, Moore RA, Sumatriptan plus naproxen for the treatment of acute migraine attacks in adults, Cochrane Database Syst Rev, 2016; 4CD008541
- « Patient bleeds dark green blood », BBC News, (lire en ligne, consulté le )
- (en) Tablets
- (en) Drugs of the Future, 1989, 14, 35-39.
- (en) DOI 10.3987/COM-97-8087
- (en) DOI 10.3987/COM-99-8815
Liens externes
modifier- Compendium suisse des médicaments : spécialités contenant Sumatriptan