Sitagliptine
La sitagliptine est une molécule antidiabétique, de la classe des inhibiteurs de dipeptidyl peptidase-4 (DPP4) ou gliptines.
| Sitagliptine | ||
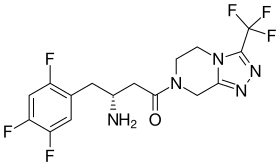
| ||
 | ||
| Identification | ||
|---|---|---|
| Nom UICPA | (3R)-3-amino-1-[3-(trifluorométhyl)-5,6-dihydro[1,2,4]triazolo[4,3-a]pyrazin-7(8H)-yl]-4-(2,4,5-trifluorophényl)butan-1-one | |
| Synonymes |
(R)-4-oxo-4-[3-(trifluorométhyl)-5,6-dihydro[1,2,4]triazolo[4,3-a]pyrazin-7(8H)-yl]-1-(2,4,5-trifluorophényl)butan-2-amine |
|
| No CAS | ||
| No ECHA | 100.217.948 | |
| Code ATC | A10 | |
| DrugBank | DB01261 | |
| PubChem | 4369359 | |
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | C16H15F6N5O [Isomères] |
|
| Masse molaire[1] | 407,313 6 ± 0,015 2 g/mol C 47,18 %, H 3,71 %, F 27,99 %, N 17,19 %, O 3,93 %, |
|
| Données pharmacocinétiques | ||
| Biodisponibilité | 87 % | |
| Liaison protéique | 38 % | |
| Métabolisme | hépatique | |
| Demi-vie d’élim. | 8 à 14 h[2] | |
| Excrétion | ||
| Considérations thérapeutiques | ||
| Voie d’administration | oral | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
Mode d'action
modifierLa sitagliptine inhibe la DPP4 qui dégrade les incrétines, d'où une augmentation de leur effet.
Indication
modifierElle permet d'aider à équilibrer le diabète de type 2 sans toutefois démontrer d'efficacité quant à la diminution du risque principal de cette maladie, qui est la survenue d'une maladie cardiovasculaire[3].
Elle permet, en association avec le tacrolimus et le sirolimus de diminuer le risque d'une réaction du greffon contre l'hôte[4],[5],[6]
Spécialité contenant de la sitagliptine
modifier- Januvia comprimés
- Xelevia comprimés
- Janumet comprimés pelliculés
- Velmetia comprimés pelliculés
Effets secondaires
modifierIl existe un risque de survenue d'une pancréatite aiguë[7].
En 2013, deux études associant les incrétines et les gliptines à un risque accru de pancréatite et de métaplasie des cellules ductales[Note 1] ont été publiées[8],[9] ce qui a amené la Food and Drug Administration (FDA) aux États-Unis[10],[11] puis l'Agence européenne des médicaments à demander des investigations complémentaires sur les risques pancréatiques des traitements basés sur ces molécules dans le diabète de type 2[12].
En Europe, les molécules impliquées dans ces demandes de recherche complémentaire sont : l'exénatide (Byetta, Bydureon), la liraglutide (Victoza), la lixisénatide (Lyxumia), la sitagliptine (Efficib, Januvia, Janumet, Ristaben, Ristfor, Tesavel, Velmetia, Xelevia), la saxagliptine (Komboglyze, Onglyza), la linagliptine (Jentadueto, Trajenta) et la vildagliptine (Eucreas, Galvus, Icandra, Jalra, Xiliarx, Zomarist).
Liens externes
modifier- Compendium suisse des médicaments : spécialités contenant Sitagliptine
Notes et références
modifierNotes
modifier- Le pancréas exocrine est formé de deux types cellulaires, les cellules acineuses et les cellules canalaires ou ductales.
Références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Herman G, Stevens C, Van Dyck K, Bergman A, Yi B, De Smet M, Snyder K, Hilliard D, Tanen M, Tanaka W, Wang A, Zeng W, Musson D, Winchell G, Davies M, Ramael S, Gottesdiener K, Wagner J, « Pharmacokinetics and pharmacodynamics of sitagliptin, an inhibitor of dipeptidyl peptidase IV, in healthy subjects: results from two randomized, double-blind, placebo-controlled studies with single oral doses. », Clin. Pharmacol. Ther., vol. 78, no 6, , p. 675–88 (PMID 16338283, DOI 10.1016/j.clpt.2005.09.002)
- Green JB, Bethel MA, Armstrong PW et al. Effect of sitagliptin on cardiovascular outcomes in type 2 diabetes, N Engl J Med, 2015;373:232-242
- Farag SS, Abu Zaid M, Schwartz JE et al. Dipeptidyl peptidase 4 inhibition for prophylaxis of acute graft-versus-host disease, N Engl J Med, 2021;384:11-19
- Paul J. Martin Sitagliptin to Prevent Acute Graft-versus-Host Disease N Engl J Med 2021; 384:70-71 DOI: 10.1056/NEJMe2032581
- Dennis L. Cooper et Coll Sitagliptin for Prophylaxis of Acute Graft-versus-Host Disease N Engl J Med 2021; 384:1374-1376 https://www.nejm.org/doi/full/10.1056/NEJMc2101975?query=TOC
- Singh S, Chang H-Y, Richard TM, Weiner JP, Clark JM, Segal JB, Glucagonlike peptide 1-based therapies and risk of hospitalization for acute pancreatitis in type 2 diabetes mellitus: a population-based matched case-control study, JAMA Intern Med, 2013
- (en) (en) S. Singh, H.Y. Chang, T.M. Richards, J.P. Weiner, J.M. Clark, J.B. Segal, « Glucagonlike Peptide 1-Based Therapies and Risk of Hospitalization for Acute Pancreatitis in Type 2 Diabetes Mellitus: A Population-Based Matched Case-Control Study », JAMA internal medicine, vol. 173, no 7, , p. 1-6 (PMID 23440284, DOI 10.1001/jamainternmed.2013.2720, lire en ligne [html], consulté le )
- (en) (en) A.E Butler, M. Campbell-Thompson, T. Gurlo, D.W. Dawson, M. Atkinson, P.C. Butler, « Marked Expansion of Exocrine and Endocrine Pancreas with Incretin Therapy in Humans with increased Exocrine Pancreas Dysplasia and the potential for Glucagon-producing Neuroendocrine Tumors », Diabetes, vol. 62, no 7, , p. 2595-2604 (PMID 23524641, PMCID PMC3712065, DOI 10.2337/db12-1686, lire en ligne [html], consulté le )
- Alerte FDA 2008
- Alerte FDA 2009
- [PDF](en) Communiqué de presse EMA