Oléandrine
L'oléandrine est un hétéroside cardiotonique, principal poison extrait du Laurier-rose (Nerium oleander). Elle est présente dans toutes les parties de la plante. L'intoxication à l'oléandrine est souvent mortelle.
| Oléandrine | |||
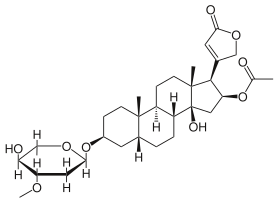
| |||
| Structure en représentation de Haworth de l'oléandrine | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | acétate de [(3S,5R,8R,9S,10S,13R,14S,16S,17R)-14-hydroxy-3-[(2R,4S,5S,6S)-5-hydroxy-4-méthoxy-6-méthyloxan-2-yl]oxy-10,13-diméthyl-17-(5-oxo-2H-furan-3-yl)-1,2,3,4,5,6,7,8,9,11,12,15,16,17-tétradécahydrocyclopenta[a]phénanthrén-16-yle] | ||
| Synonymes |
oléandroside, foliandrine, folinérine, nériostène, nérioline |
||
| No CAS | |||
| No ECHA | 100.006.693 | ||
| No CE | 207-361-5 | ||
| No RTECS | FH4585000 | ||
| PubChem | 11541511 | ||
| SMILES | |||
| InChI | |||
| Apparence | poudre blanche à blanchâtre[1] | ||
| Propriétés chimiques | |||
| Formule | C32H48O9 [Isomères] |
||
| Masse molaire[2] | 576,718 1 ± 0,031 7 g/mol C 66,64 %, H 8,39 %, O 24,97 %, |
||
| Propriétés physiques | |||
| T° fusion | 250 °C[3] | ||
| Solubilité | sol. in éthanol, chloroforme[3]; Quasiment insoluble dans l'eau [4] | ||
| Propriétés optiques | |||
| Pouvoir rotatoire | = -48,0° (cc= 1,3 in méthanol)[3] | ||
| Précautions | |||
| SGH[1] | |||
| H300, H330, H373, P260, P264, P284, P310 et P301+P310 |
|||
| Transport[1] | |||
|
|||
| Ingestion | Toxique (cardiotoxique) | ||
| Données pharmacocinétiques | |||
| Biodisponibilité | ~30%[3] | ||
| Demi-vie d’élim. | 2,3 ± 0,5 h[3] | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Elle est très proche dans sa structure et dans ses effets, de la digitaline, extraite de la digitale (Digitalis purpurea), et partage ses propriétés cardiotoxiques.
Chimie
modifierL'oléandrine est un hétéroside ; son ose est l'oléandrose[5],[6] (didésoxyarabinose), et son aglycone est un cardénolide, l'oléandrigénine, qui présente une structure de stéroïde avec un cycle insaturé de lactone en C17, également substituée par un groupe acétyloxy en C16. Elle se présente sous la forme d'un solide cristallin soluble dans les solvants polaires.
Pharmacologie
modifierL'oléandrine est plutôt bien absorbée dans le tube digestif, ce qui la rend extrêmement dangereuse en cas d'ingestion. L'intoxication est le plus souvent accidentelle[7]. L'ingestion d'une simple feuille de Laurier-rose peut être mortelle pour un adulte et un enfant[8],[9].
À l'instar des autres cardiotoxiques hétérosides, les digitaliques comme la digitoxine ou la convalatoxine, l'oléandrine inhibe la pompe membranaire Na+/K+,ATPase, ce qui génère une hyperkaliémie et provoque donc une augmentation de la force de contraction musculaire, mais retarde la repolarisation[10],[11]. Elle ralentit fortement le rythme cardiaque. Elle provoque un déséquilibre ionique au niveau cardiaque, ce qui mène à l'arrêt cardiaque[10].
Après ingestion, un tableau clinique typique est souvent décrit, associant signes digestifs et neurologiques[12],[13],[14],[15] :
- nausées et vomissements ;
- douleur abdominale ;
- phosphènes ;
mais surtout des effets cardiovasculaires :
- arythmie ventriculaire ;
- bradycardie ;
- fibrillation atriale ;
- bloc atrio-ventriculaire ;
- hyperkaliémie ;
- arrêt cardiorespiratoire.
Ces symptômes sont traités par l'administration d'atropine et par le lavage gastrique au charbon activé.
Les symptômes sont souvent très graves et souvent résistants aux nombreux traitements[16].
La détection de l'oléandrine dans la circulation sanguine est difficile, fait appel à l'immuno-enzymo-fluorimétrie et un faux résultat positif pour la digitoxine est souvent observé[17],[18], due à une réactivité croisée, et à la proximité de structure entre les deux molécules.
Pour ces raisons, l'intoxication à l'oléandrine, et plus généralement l'ingestion de laurier-rose, est presque toujours mortelle[19].
L'oléandrine est également un modulateur possible du NF-κB[20],[21], et possède une activité cytotoxique importante[22]. De fait, elle est étudiée et utilisée dans le traitement des tumeurs et montre une certaine activité dans le traitement de cancers[23],[24], in vitro, chez l'animal , et chez l'humain, sous le nom commercial de Anvirzel[25].
Historique
modifierEn 1808, durant la campagne d'Espagne, lors d'un bivouac, des soldats de Napoléon font rôtir des agneaux sur des broches de Laurier-rose. Sur les 12 soldats, 8 meurent, les 4 autres sont gravement intoxiqués[26].
Notes et références
modifier- Fiche Sigma-Aldrich du composé Oleandrin ≥98% (HPLC), consultée le 18 octobre 2017. + (pdf) Fiche MSDS
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- PubChem CID 11541511
- O'Neil, M.J. (ed.). The Merck Index - An Encyclopedia of Chemicals, Drugs, and Biologicals. Cambridge, UK: Royal Society of Chemistry, 2013., p. 1265
- (en) Pubchem, « Corrigen », sur pubchem.ncbi.nlm.nih.gov (consulté le )
- René Milcent et François Chau, Chimie organique hétérocyclique (Structures fondamentales), EDP Sciences, , 846 p. (ISBN 978-2-7598-0174-9, lire en ligne)
- Luigi Papi, Alessandro Bassi Luciani, David Forni et Mario Giusiani, « Unexpected double lethal oleander poisoning », The American Journal of Forensic Medicine and Pathology, vol. 33, no 1, , p. 93–97 (ISSN 1533-404X, PMID 21926903, DOI 10.1097/PAF.0b013e31822d33d4, lire en ligne, consulté le )
- « Informations sur l'intoxication: laurier-rose », Système canadien d'information sur la biodiversité.
- « Laurier-rose », École nationale vétérinaire de Lyon.
- Ana Flávia Machado Botelho, Artur Santos-Miranda, Humberto Cavalcante Joca et Cláudio Roberto Scabelo Mattoso, « Hydroalcoholic extract from Nerium oleander L. (Apocynaceae) elicits arrhythmogenic activity », Journal of Ethnopharmacology, vol. 206, , p. 170–177 (ISSN 1872-7573, PMID 28564584, DOI 10.1016/j.jep.2017.05.031, lire en ligne, consulté le )
- Bors G et al; Toxicology of Nerium oleander; Pharmazie 26 (12) 764 (1971)
- Grant, W.M, « Toxicology of the Eye », 3rd ed. Springfield, IL: Charles C. Thomas Publisher, , p. 675
- Pietro Palmisano, Yusef Hadad, De Nuccio et Fernando Antonio, « An unusual case of oleandrin poisoning suggesting its possible antiarrhythmic activity », EP Europace, vol. 17, no 9, , p. 1401–1401 (ISSN 1099-5129, DOI 10.1093/europace/euv050, lire en ligne, consulté le )
- Işıl Bavunoğlu, Musa Balta et Zeynep Türkmen, « Oleander Poisoning as an Example of Self-Medication Attempt », Balkan Medical Journal, vol. 33, no 5, , p. 559–562 (ISSN 2146-3123, PMID 27761287, PMCID PMC5056662, DOI 10.5152/balkanmedj.2016.150307, lire en ligne, consulté le )
- Cecilia Gechtman, Federico Guidugli, Alessandro Marocchi et Adriano Masarin, « Unexpectedly dangerous escargot stew: oleandrin poisoning through the alimentary chain », Journal of Analytical Toxicology, vol. 30, no 9, , p. 683–686 (ISSN 0146-4760, PMID 17137529, lire en ligne, consulté le )
- J. Osterloh, S. Herold et S. Pond, « Oleander interference in the digoxin radioimmunoassay in a fatal ingestion », JAMA, vol. 247, no 11, , p. 1596–1597 (ISSN 0098-7484, PMID 7038154, lire en ligne, consulté le )
- P. Datta , A. Dasgupta, Interference of Oleandrin andOleandrigenin in digitoxin immunoassays : minimal cross reactivity with a new monoclonal chemiluminescent assay and high cross reactivity with the fluorescence polarization assay, Ther. Drug. Monit., 1997, vol. 19(4), pp. 465-469
- Mustapha Moulsma, Éric Lacassie, Isabelle Boudre et Jean-Michel Gaulier, « A propos d'un cas d'intoxication volontaire au Laurier rose (Nerium oleander L., Apocynaceae) », Annales de Toxicologie Analytique, vol. 12, no 2, , p. 122–130 (ISSN 0996-8423, DOI 10.1051/ata/2000018, lire en ligne, consulté le )
- Ibrahim A. Wasfi, Omar Zorob, Nawal A. Al katheeri et Anwar M. Al Awadhi, « A fatal case of oleandrin poisoning », Forensic Science International, vol. 179, nos 2-3, , e31–36 (ISSN 1872-6283, PMID 18602779, DOI 10.1016/j.forsciint.2008.05.002, lire en ligne, consulté le )
- Yashin Sreenivasan, Abira Sarkar et Sunil Kumar Manna, « Oleandrin suppresses activation of nuclear transcription factor-kappa B and activator protein-1 and potentiates apoptosis induced by ceramide », Biochemical Pharmacology, vol. 66, no 11, , p. 2223–2239 (ISSN 0006-2952, PMID 14609747, lire en ligne, consulté le )
- Nune Raviprakash et Sunil Kumar Manna, « Short-term exposure to oleandrin enhances responses to IL-8 by increasing cell surface IL-8 receptors », British Journal of Pharmacology, vol. 171, no 14, , p. 3339–3351 (ISSN 0007-1188, PMID 24172227, PMCID PMC4105924, DOI 10.1111/bph.12493, lire en ligne, consulté le )
- Arvind Kumar, Tanmoy De, Amrita Mishra et Arun K. Mishra, « Oleandrin: A cardiac glycosides with potent cytotoxicity », Pharmacognosy Reviews, vol. 7, no 14, , p. 131–139 (ISSN 0973-7847, PMID 24347921, PMCID PMC3841991, DOI 10.4103/0973-7847.120512, lire en ligne, consulté le )
- Stefano Garofalo, Alfonso Grimaldi, Giuseppina Chece et Alessandra Porzia, « The Glycoside Oleandrin Reduces Glioma Growth with Direct and Indirect Effects on Tumor Cells », The Journal of Neuroscience: The Official Journal of the Society for Neuroscience, vol. 37, no 14, , p. 3926–3939 (ISSN 1529-2401, PMID 28292827, DOI 10.1523/JNEUROSCI.2296-16.2017, lire en ligne, consulté le )
- Robert A. Newman, Yasuko Kondo, Tomohisa Yokoyama et Susan Dixon, « Autophagic cell death of human pancreatic tumor cells mediated by oleandrin, a lipid-soluble cardiac glycoside », Integrative Cancer Therapies, vol. 6, no 4, , p. 354–364 (ISSN 1534-7354, PMID 18048883, DOI 10.1177/1534735407309623, lire en ligne, consulté le )
- S. Pathak, A. S. Multani, S. Narayan et V. Kumar, « Anvirzel, an extract of Nerium oleander, induces cell death in human but not murine cancer cells », Anti-Cancer Drugs, vol. 11, no 6, , p. 455–463 (ISSN 0959-4973, PMID 11001386, lire en ligne, consulté le )
- Le Livre des plantes médicinales et vénéneuses de France, A. Fournier, Paris, 1948. p. 397.



