Liposome
Un liposome est une vésicule artificielle formée par des bicouches lipidiques concentriques, emprisonnant entre elles des compartiments aqueux. On en obtient à partir d'une grande variété de lipides amphiphiles, dont les plus souvent des phospholipides. Lorsque de tels composés sont mis en présence d'un excès de solution aqueuse, ils s'organisent de manière à minimiser les interactions entre leurs chaînes hydrocarbonées et l'eau. La formation de ces vésicules a été mise en évidence par Alec Bangham en 1965.
Les liposomes ont une taille nanométrique et sont principalement utilisés dans la thérapie des cancers ou de maladies respiratoires. Le premier liposome commercialisé fut le Doxil. Depuis, une dizaine de liposomes ont atteint le marché de la santé. Des « nanoliposomes » sont produits par les nanotechnologies[1], visant notamment le marché des produits alimentaires[1] et celui des nanomédicaments, pour délivrer des oligonucléotides de manière ciblée[2].
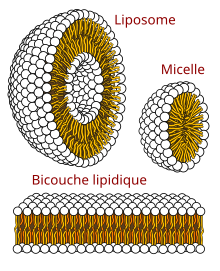
Caractéristiques
modifierTaille
modifierEn milieux aqueux, les phospholipides naturels forment spontanément des liposomes. La taille des liposomes est à l'échelle du nanomètre, ayant un diamètre de 20 à plus de 1000 nm[3].
Configuration et mouvements
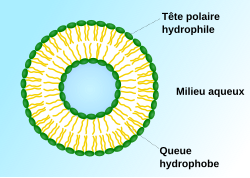
modifierLa bicouche de phospholipides sépare le milieu intravésiculaire du milieu extérieur aqueux. Les têtes polaires des phospholipides sont à l'extérieur et les queues apolaires sont au bord du milieu intérieur, minimisant ainsi les interactions entre les composantes hydrophobes[3].
Les phospholipides ne sont pas fixés, leurs mouvements sont identiques à ceux dans les membranes biologiques.
Passage des solutés
modifierSeules certaines molécules peuvent passer au travers des bicouches. Par exemple, les macromolécules ne peuvent pas passer, mais les petits solutés hydrophiles et certains solutés hydrophobes peuvent passer librement à travers la bicouche[3].
Mouvements des lipides dans un liposome
modifierLa rotation autour des liaisons C-C des chaînes hydrocarbonées change la configuration des chaînes qui passent alors de cis à gauche ou vice-versa. La configuration la plus stable est la configuration trans, ou β, alors que la configuration cis, ou ɑ, est moins stable. Dans la configuration β, les chaînes sont plus étirées, ordonnées et séparées d’une distance moins grande grâce à plus d’interactions hydrophobes entre les queues phospholipides. Par contre, la configuration ɑ est moins stable à cause de la séparation entre les chaines hydrophobes des queues lipidiques[3].
Avec plus de liaisons cis, les membranes sont plus désordonnées et plus fluides. Par contre, avec moins de liaisons cis, la conformation β est plus ordonnée et moins fluide. Cette relation est plus importante avec les phospholipides courts qu’avec les phospholipides longs[3].
Température de transition (Tc)
modifierLa transition de la configuration alpha à la configuration beta nécessite une température plus haute qui entraîne la rotation des liaisons C-C[3].
La température de transition dépend de la longueur des chaînes et de la saturation des chaînes. En effet, avec plus de carbones dans la chaîne acyle, il y a plus d’interactions entre lipides, donc la température de transition augmente avec les chaines plus longues. Deuxièmement, une moindre saturation des chaînes veut dire qu’il y a moins d’interactions entre lipides parce qu’il y a plus de configurations cis. Donc, la température de transition diminue au fur et à mesure que le nombre d’insaturations augmente[3].
Les différents types de liposomes
modifierOn les classe selon leur taille et le nombre de compartiments :
- les liposomes multilamellaires ou MLV (multilamellar Vesicle) ;
- les petits liposomes unilamellaires ou SUV (small unilamellar Vesicle) ;
- les gros liposomes unilamellaires ou LUV (large unilamellar Vesicle) ;
- les liposomes unilamellaires géants ou GUV (giant unilamellar Vesicle).
L'industrie cosmétique a mis au point des liposomes synthétiques, les Niosomes (brevet L'OREAL), dont la paroi n'est plus constituée de phospholipides mais de lipides non ioniques. On doit à Vanlerberghe, G. et ses collaborateurs (1978) la découverte de cette famille de composés non ioniques, les lipopolyglycérols comportant une seule chaîne hydrocarbonée (chaîne C12-C18), ou niosomes, qui présentent le même type d’organisation que les phospholipides.
Synthèse des liposomes
modifierLes liposomes sont préparés à partir de phospholipides. Il y a une organisation de ces phospholipides dans un état thermodynamiquement stable tel que les têtes polaires se regroupent entre elles et permettent l'établissement d'une bicouche. Cette bicouche peut être constituée d'un seul ou plusieurs types de phospholipides naturels ou de synthèse.
La façon la plus classique de préparer des liposomes est celle dite de l'hydratation d'un film lipidique. Ce film est souvent obtenu par évaporation d'un solvant organique dans lequel les lipides étaient dissous. L'hydratation de ce film conduit alors à une séparation de morceaux de bicouche. Les liposomes ne se forment qu’à une température supérieure à celle de leur transition de phase, donc cette étape doit être faite à une température supérieure ou égale à la température de transition de phase (Tc).
Les morceaux forment ce que l'on appelle des MLV (multi lamellar vesicle) qui peuvent ensuite être transformés (calibrage à une certaine taille ou élimination de couches multiples) par une extrusion.
Souvent les étapes supplémentaires ci-dessous sont accomplies pour obtenir des vésicules unilamellaires :
Les liposomes sont soniqués à basse fréquence durant un temps court sous atmosphère d’azote ou d’argon. Ensuite, les liposomes sont centrifugés pour séparer par le poids les MLV des SUV et des LUV. Puis des cycles de congélation et décongélation sont utilisés pour fragiliser la membrane et pour créer les liposomes unilamellaires. Finalement, les MLV résiduels et les LUV de trop grande taille peuvent être séparés par filtration avec un pore de 100 nm[3].
Évolution des liposomes pour en faire des vecteurs furtifs et spécifiques
modifierPremière génération
modifierL'utilisation de phospholipides naturels permet de créer des systèmes qui miment les membranes biologiques, ce qui fut d'ailleurs la première utilisation des liposomes.
La présence à la fois d'une partie hydrophobe et d'une partie hydrophile a ensuite été utilisée pour formuler des principes actifs médicamenteux.
Ils ont une structure très proche de celle des membranes cellulaires, ce qui leur permet de fusionner avec elles en libérant le ou les principes actifs qu'ils contiennent.
Seconde génération
modifierDes améliorations peuvent être apportées à ce système, comme la « PEGylation » qui consiste en l'introduction de chaînes de polyéthylène glycol (PEG) souvent greffées sur des phospholipides ou du cholestérol. Ce PEG permet une stabilisation stérique du liposome et limite l'adsorption de molécules de reconnaissance du système immunitaire (les opsonines) ce qui augmente considérablement le temps de séjour dans le système vasculaire de ces liposomes dits de seconde génération et permet ainsi de limiter les injections ou même d'envisager des thérapies ciblées.
Troisième génération
modifierLes liposomes de troisième génération, associent cette stabilisation stérique à un ciblage de la zone d'intérêt pour le traitement envisagé. La plupart du temps, des anticorps spécifiques du tissu vers lequel on souhaite diriger le liposome sont greffés au bout des chaînes de polyéthylène glycol (PEG). Il y a donc alors mise en jeu de l'affinité de l'anticorps pour l'antigène du tissu et on peut ainsi espérer une augmentation de la quantité de liposome au niveau du site d'intérêt pour le traitement.
Applications médicales
modifierLes liposomes sont de plus en plus développés dans la recherche pharmaceutique comme vecteurs de médicaments. Le premier liposome a été mis sur le marché il y a vingt ans, il s'agit du doxil qui transporte la doxorubicine, permettant de réduire sa toxicité cardiaque. Leur utilisation première est le ciblage de principes actifs. Les liposomes peuvent retenir plusieurs types de composés qu’ils soient hydrosolubles (encapsulés dans la phase aqueuse) ou liposolubles ou amphiphiles (empaquetés dans la bicouche lipidique).
Avantages d'encapsulation des médicaments dans les liposomes
modifierL’encapsulation permet la protection des substances contenues dans les liposomes vis-à-vis d’une dégradation enzymatique ou bien d’une élimination par le système immunitaire. L’encapsulation permet aussi de limiter l’action toxique des substances vis-à-vis du patient. Les liposomes permettent le passage de substances hydrosolubles à travers la barrière hydrophobe.
L'administration médicale
modifierLes liposomes sont généralement administrés par voie intraveineuse. L’administration par voie orale peut être possible. Cependant de nombreuses substances ne sont pas absorbées par le système gastro-intestinal et donc par voie orale.
Les liposomes sont également utilisés dans le cas d’applications dermatologiques et cosmétiques, car ils permettent la délivrance cutanée voire transcutanée de molécules hydrophobes et/ou hydrophiles, sans limitation de leur masse moléculaire.
Applications thérapeutiques
modifierLes liposomes peuvent véhiculer des médicaments par simple injection. Dans la circulation sanguine, ils fusionnent avec les membranes cellulaires ou sont endocytosés par les cellules pour délivrer le principe actif. Le principe actif peut être libéré lentement et de manière continue. Par exemple, on peut mettre de la morphine (amphiphile) entre les parois d’un liposome multilamellaire. Chaque fois qu’une couche se brise, un peu de médicament est libéré. Cette méthode réduit la concentration locale du médicament et donc la toxicité et les effets secondaires. L’addition de polyéthylène glycol (PEG) augmente le temps de circulation en évitant l’opsonisation par le système immunitaire[3].
Dans la thérapie génique, les liposomes encapsulent un gène ou un plasmide. Le liposome fusionne avec l’endosome, permettent la libération de l’ADN, qui peut donc être exprimé dans la cellule. Un promoteur de fusion permet la meilleure intégration possible dans les cellules cibles, tel qu’une glycoprotéine virale de surface. De plus, les liposomes sont sensibles au pH, ce qui leur permet de fusionner facilement avec les lysosomes, qui ont un pH acide. Donc ils libèrent le matériel génétique dans le cytoplasme de la cellule quand ils sont endocytosés. Les limitations à l’emploi de liposomes comme vecteurs de matériel génétique incluent des problèmes avec le ciblage du noyau et le temps d’expression du gène, qui est souvent trop court[3].
Les liposomes qui ont des glycoprotéines virales à leur surface sont appelés les « virosomes ». Ils sont captés par les macrophages, qui exposent donc directement l’agent antigène. De cette façon, les virosomes pourraient fonctionner comme des vaccins. Cette méthode est actuellement à l’étude par des chercheurs et médecins parce que les virosomes actionnent le système immunitaire tout en ne contenant pas de matériel génétique infectieux[3].
D'autres applications médicales
modifier- Les liposomes sont utilisés pour encapsuler des médicaments anticancéreux, comme le Doxil qui fut le premier médicament basé sur des liposomes accepté et commercialisé (1995) qui transporte la doxorubicine.
- L'antibiotique antifongique: l'Amphotéricine B', utilise une formule liposomale (c-i-e, utilisant dans les liposomes), nommée lAmBisome, pour traiter les infections fongiques sévère.
- Les liposomes peuvent être utilisés comme agents neutralisant des toxines bactériennes ayant évolué pour cibler les lipides présent dans la membrane cellulaire[4].
- L'industrie cosmétique utilise les liposomes comme vecteur pour véhiculer les filtres chimiques de protection solaire au cœur de l'épiderme et ainsi lui octroyer une plus longue rémanence, et ainsi éviter de réappliquer toutes les 2 heures (ex. : Daylong, à 1 seule application par jour).
- Dans les années 1980, les laboratoires RoC ont été les premiers à intégrer des liposomes à une crème de soin pour le visage[5].
- Les liposomes sont aussi utilisés en imagerie médicale par introduction de substances fluorescentes ou radiomarquées et permettent de suivre l’accumulation de ces substances.
Notes et références
modifier- M. Reza Mozafari & al. (2008), Nanoliposomes and Their Applications in Food Nanotechnology, Journal of Liposome Research, 18:309–327, 2008; (ISSN 0898-2104) print / 1532-2394 online ; DOI:10.1080/08982100802465941.
- (en) Meenu Mehta, Deeksha, Devesh Tewari et Gaurav Gupta, « Oligonucleotide therapy: An emerging focus area for drug delivery in chronic inflammatory respiratory diseases », Chemico-Biological Interactions, vol. 308, , p. 206–215 (PMID 31136735, PMCID PMC7094617, DOI 10.1016/j.cbi.2019.05.028, lire en ligne, consulté le ).
- Aurélien Lorin, Christelle Flore, Annick Thomas et Robert Brasseur, « Les liposomes : description, fabrication et applications », Biotechnol. Aaron. Soc. Environ, no 8, , p. 163-176 (lire en ligne).
- (en) « Besançon et al., 2021 Tailored liposomal nanotraps for the treatment of Streptococcal infections. J Nanobiotechnol », (consulté le ).
- (en) « ROC celebrates 50 innovate years with new products for 2007 », sur ELIXIR, (consulté le ).
Articles connexes
modifierLiens externes
modifier- (fr) Nanotechnologies et Santé, dossier Sagascience du CNRS
- (fr) Chimie et Beauté, dossier Sagascience du CNRS
- (fr) Les Liposomes : description, fabrication et applications, article dans la revue Biotechnologie, Agronomie, Société et Environnement
- (fr) Animation sur la vectorisation, dossier Sagascience du CNRS
- (fr) Problématiques de la vectorisation
- (fr) Le concept de vectorisation
- (fr) La Nanotechnologie appliquée au Cancer