Hémoglobine fœtale
L'hémoglobine fœtale (ou HbF) est un type d'hémoglobine synthétisé chez le fœtus et le nouveau-né et disparaissant par la suite, sauf lors de certaines maladies.
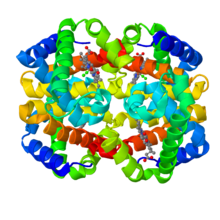
Structure
modifierIl s'agit d'une hémoglobine α2γ2, contenant deux sous-unités γ et deux sous unités α. Pour mémoire, l'hémoglobine adulte est de type α2β2. Cette hémoglobine est totalement fonctionnelle pour le transport de l'oxygène. Son affinité pour l'oxygène comparativement à l'hémoglobine adulte est supérieure. Ceci résulte de la diminution d'affinité pour le 2,3-bisphosphoglycérate (2,3-BPG). Cet acide stabilise la désoxyhémoglobine car sa forte charge négative interagit bien avec la chaine bêta de l'hémoglobine adulte et favorise la dissociation de l'oxygène. La chaîne γ de l'hémoglobine ne contient pas une charge aussi positive car elle contient un résidu d'histidine en moins.
Le gène
modifierLe gène codant la globine γ est situé, chez l'être humain sur le chromosome 11, à peu de distance de celui codant la globine β.
Persistance de l'hémoglobine fœtale à l'âge adulte
modifierElle peut se trouver de manière isolée, dans le cadre d'un syndrome de persistance de l'hémoglobine fœtale à l'âge adulte. Elle peut être synthétisée également en cas d'anomalie de l'hémoglobine, par exemple, en cas de thalassémie.
La persistance de sa production semble améliorer plusieurs hémoglobinopathies, dont la thalassémie bêta[1] et la drépanocytose[2].
Le BCL11A est un facteur de transcription qui inhibe la production d'hémoglobine fœtale[3].
Cible thérapeutique
modifierUne thérapie génique permet de réactiver la production d'hémoglobine foetale avec une amélioration considérable des symptômes de la drépanocytose[4]. Lors d'une thalassémie bêta, elle annule pratiquement les besoins transfusionnels[5].
Notes et références
modifier- Fessas P, Stamatoyannopoulos G, Hereditary persistence of fetal hemoglobin in Greece: a study and a comparison [archive], Blood, 1964;24:223-240
- Platt OS, Brambilla DJ, Rosse WF et al. Mortality in sickle cell disease — life expectancy and risk factors for early death [archive], N Engl J Med, 1994;330:1639-1644
- Sankaran VG, Menne TF, Xu J et al. Human fetal hemoglobin expression is regulated by the developmental stage-specific repressor BCL11A [archive], Science, 2008;322:1839–1842
- Frangoul H, Locatelli F, Sharma A et al. Exagamglogene autotemcel for severe sickle cell disease [archive], N Engl J Med, 2024;390:1649-1662
- Locatelli F, Lang P, Wall D et al. Exagamglogene autotemcel for transfusion-dependent β-thalassemia [archive], N Engl J Med, 2024;390:1663-1676