Gemcitabine
La gemcitabine est la dénomination commune internationale de l'isomère β de la 2'-désoxy-2',2'-difluorocytidine. Son chlorhydrate est utilisé comme médicament antimétabolite qui après phosphorylations s'incorpore dans l'ADN en mimant la cytidine et inhibe la synthèse nucléotidique ce qui entraine la mort cellulaire.
| Gemcitabine | |
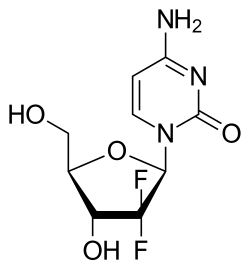
| |
| Identification | |
|---|---|
| Nom UICPA | 2'-deoxy-2',2'-difluorocytidine |
| No CAS | (base) et (chlorhydrate) |
| No ECHA | 100.124.343 |
| Code ATC | L01 |
| Propriétés chimiques | |
| Formule | C9H11F2N3O4 [Isomères] |
| Masse molaire[1] | 263,198 1 ± 0,009 8 g/mol C 41,07 %, H 4,21 %, F 14,44 %, N 15,97 %, O 24,32 %, |
| Données pharmacocinétiques | |
| Métabolisme | déamination en un dérivé de l'uracile (inactif) |
| Demi-vie d’élim. | rapide : de l'ordre de l'heure |
| Considérations thérapeutiques | |
| Classe thérapeutique | Immunosuppresseur |
| Voie d’administration | injectable |
| Grossesse | précautions des cytostatiques |
| Précautions | Belgique : sous ordonnance (certaines formes sont réservées à l'usage hospitalier) |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La gemcitabine est utilisée dans le traitement chimiothérapeutique du cancer du pancréas, du cancer du poumon non à petites cellules (NSCLC), du cancer du sein et du cancer de la vessie.
Elle a reçu sa première autorisation de mise sur le marché en 1996 en France dans le traitement du cancer du pancréas.
| (Chlorhydrate de) gemcitabine | |
| Informations générales | |
|---|---|
| Princeps |
|
| Classe | Immunosuppresseur |
| Identification | |
| No CAS | |
| No ECHA | 100.124.343 |
| Code ATC | L01BC05 |
| DrugBank | DB00441 |
| modifier |
|
Historique
modifierUn composé anticancéreux, la cytarabine, a été largement utilisée depuis les années 1950 dans le traitement des leucémies[réf. nécessaire] et des équipes se sont lancées dans la recherche de composés analogues.
Au début des années 1980, Joseph H. Burchenal travaillant au Memorial Sloan-Kettering Cancer Center à New York démontre à partir de la cytarabine que la substitution d'un atome d'hydrogène en position 2' par un atome de fluor résulte en un composé fortement cytotoxique[réf. nécessaire].
Dans le même temps, en 1980 Gerald Grindey, pharmacologue reconnu, rejoint les laboratoires Eli Lilly à Indianapolis et lance un nouveau programme de recherche de composés anticancéreux, en particulier de nouveaux antimétabolites. Larry Hertel, un chimiste travaillant dans son équipe reprenant l'idée de Burchenal, a alors l'idée d'ajouter non pas un mais deux atomes de fluor en position 2', aboutissant à ce qui deviendra la gemcitabine[2]. Ce composé a été synthétisé dans le but d'être actif comme agent antiviral. Cependant, en 1990, il a été rapporté une activité anticancéreuse de la 2'-désoxy-2',2'-difluorocytidine (gemcitabine) sur des cellules leucémiques en culture[3]. Par la suite, des études cliniques ont été menées et la gemcitabine a obtenu son autorisation de mise sur le marché au milieu des années 1990, d'abord au Royaume Uni en 1995 et en France en 1996.
Mécanisme d'action
modifierLa gemcitabine est un antimétabolite pyrimidique. Elle doit subir plusieurs phosphorylations par une kinase intracellulaire pour former le composé triphosphate actif.
Elle entraine une mort cellulaire en phase S de manière dose- et temps-dépendant.
Indications
modifier- Adénocarcinome du pancréas localement avancé ou métastatique
- Cancer de la vessie localement avancé ou métastatique, en association avec le cisplatine
- Carcinome épithélial de l'ovaire localement avancé ou métastatique, en association avec le carboplatine
- Cancer bronchique non à petites cellules (CBNPC) localement avancé ou métastatique en association avec le cisplatine
- Cancer du sein inopérable, localement récidivant ou métastatique, en rechute après une chimiothérapie adjuvante/néoadjuvante en association avec le paclitaxel.
Posologie
modifierLa posologie standard de gemcitabine est de 1 000 à 1 250 mg·m-2 à passer en perfusion intraveineuse sur 30 minutes.
Pharmacocinétique
modifierLa gemcitabine est rapidement métabolisée par la cytidine déaminase dans tous les tissus.
La distribution tissulaire est importante et l'excrétion est uniquement urinaire[4].
Effets indésirables
modifierLe principal effet indésirable résulte de l'action de la gemcitabine sur la moelle osseuse productrice des globules blancs, rouges et plaquettes. On retrouve une toxicité hématologique (leucopénie, neutropénie, thrombopénie, anémie). La baisse des globules blancs (leucopénie, neutropénie) pouvant induire des infections avec fièvre, frissons, myalgies).
Des sensations de malaise, sueurs et troubles du sommeil ainsi que des éruptions cutanées allergiques fréquemment associées à un prurit mais aussi des œdèmes sont rapportés. Le traitement provoque également dans certains cas une alopécie modérée dans certains cas (chute des cheveux).
Études cliniques
modifierNotes et références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Pearce HL, Alice Miller M., « The evolution of cancer research and drug discovery at Lilly Research Laboratories », Advan. Enzyme Regul, vol. 45, no 1, , p. 229-55. (PMID 16143373)
- (en) larry Hertel, « Evaluation of the Antiumor Activity of Gemcitabine », Cancer Research,
- Site E-vidal
Liens externes
modifier- Compendium suisse des médicaments : spécialités contenant Gemcitabine
- Page spécifique sur le Répertoire Commenté des Médicaments, par le Centre belge d'information pharmacothérapeutique
- Page spécifique sur le Vidal.fr