Oxyde de curium(IV)
composé chimique
(Redirigé depuis CmO2)
L'oxyde de curium(IV), encore appelé dioxyde de curium, est un composé chimique de formule CmO2. C'est un solide cristallin noir.
| Oxyde de curium(IV) | |
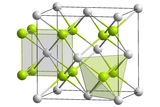
| |
| __ Cm4+ __ O2− Structure de l'oxyde de curium(IV) |
|
| Identification | |
|---|---|
| Nom UICPA | Oxyde de curium(IV) |
| Synonymes |
dioxyde de curium |
| No CAS | [1] |
| No ECHA | 100.031.453 |
| Apparence | Solide noir |
| Propriétés chimiques | |
| Formule | CmO2 |
| Masse molaire[2] | 279 g/mol Cm 88,56 %, O 11,47 %, |
| Propriétés physiques | |
| T° fusion | 380 °C (décomposition) |
| Cristallographie | |
| Système cristallin | Cubique |
| Réseau de Bravais | Cubique faces centrées |
| Classe cristalline ou groupe d’espace | Fm3m (no 225) |
| Structure type | fluorine (CaF2)[3] |
| Précautions | |
 Composé radioactif |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
On l'obtient par oxydation directe de curium métallique à l'air libre ou sous atmosphère d'oxygène :
On peut également le former à partir de l'oxyde de curium(III) Cm2O3 sous atmosphère d'oxygène à 650 °C :
Au chauffage, le dioxyde de curium commence à libérer de l'oxygène à partir de 380 °C en s'écartant de la stœchiométrie jusqu'à une formule proche de CmO1,95, avant réduction en oxyde de curium(III) Cm2O3 vers 430 °C.
Références
modifier- ↑ WebElements Curium dioxide
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ (en) Bodie E. Douglas, Shih-Ming Ho, Structure and Chemistry of Crystalline Solids, Pittsburgh, PA, USA, Springer Science + Business Media, Inc., , 346 p. (ISBN 978-0-387-26147-8, LCCN 2005927929)


