Acide tannique
L'acide tannique (Acidum tannicum), est un polyphénol de la famille des tanins hydrolysables. Il est présent dans les noix de galle, l'écorce et d'autres parties des plantes. Il est utilisé pour la clarification du vin ou de la bière et la dénaturation de l'alcool industriel. Il possède un goût astringent similaire à l'acide gallique.
| Acide tannique | ||
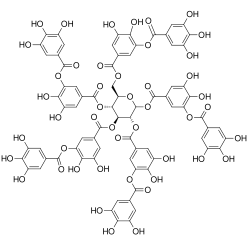
| ||
 | ||
| Une bouteille de solution aqueuse d'acide tannique. | ||
| Identification | ||
|---|---|---|
| Nom UICPA | beta-D-Glucose pentakis(3,4-dihydroxy-5-((3,4,5-trihydroxybenzoyl)oxy)benzoate) | |
| Synonymes |
acide gallotannique |
|
| No CAS | ||
| No ECHA | 100.014.321 | |
| No CE | 215-753-2 | |
| PubChem | ||
| No E | E181 | |
| FEMA | 3042 | |
| SMILES | ||
| Apparence | Poudre amorphe jaune-brun[1] | |
| Propriétés chimiques | ||
| Formule | C76H52O46 |
|
| Masse molaire[3] | 1 701,198 5 ± 0,078 2 g/mol C 53,66 %, H 3,08 %, O 43,26 %, |
|
| pKa | ~10 [2] | |
| Propriétés physiques | ||
| T° fusion | 210 °C[4] (décompose)[5] | |
| Solubilité | Soluble dans l'eau (un gramme par 0,35 mL[4]), l'Ethanol, Acétone et Alcool méthylique[5]. | |
| Masse volumique | 0,3 à 0,5[5] | |
| T° d'auto-inflammation | 526 °C[4] | |
| Point d’éclair | 198 °C[4] | |
| Précautions | ||
| NFPA 704 | ||
| Classification du CIRC | ||
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[6] | ||
| Écotoxicologie | ||
| DL50 | 5 g·kg-1 (souris, orale) & 2,26 g·kg-1 (rat, orale)[5] | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
Origine
modifierL'acide tannique est présent dans de nombreuses plantes, en particulier l'écorce du chêne[7], le Séquoia à feuilles d'if ou Tynanthus panurensis. On le trouve dans toutes les parties de la plante, graines, galle, cônes et bois.
Le chimiste Jöns Jacob Berzelius signale qu'en 1838, on utilisait l'extrait d'écorce de chêne (« quercitannate ») pour dissoudre la morphine[8].
Propriétés
modifierL'acide tannique est un dérivé de l'acide gallique, plus précisément un polyester de glucose. Il y a dix unités d'acide gallique pour un glucose.
C'est un composé jaune à marron clair fortement soluble dans l'eau (un gramme par 0,35 mL d'eau). C'est un acide faible avec un pKa autour de 10[2].
Utilisations
modifierL'acide tannique est utilisé en médecine vétérinaire comme astringent antidiarrhéique sous forme de lavements. [précision nécessaire]
L'acide tannique sert à la fabrication d'encres[1] (encre métallo-gallique) et de colorant alimentaire (E181).
Possédant un goût astringent, il est utilisé comme agent de saveur[1] (Numéro fema GRAS 3042) pour aliment et le tabac, ou dénaturant d'alcool industriel.
En gravimétrie, on utilise une solution d'acide tannique pour précipiter l'aluminium, le béryllium, le chrome, le gallium, le germanium, le niobium, l'antimoine, l'étain, le tantale, le thorium, le titane, l'uranium, la vanadium, le tungstène, le zirconium[9].
L'acide tannique est utilisé pour passiver la corrosion du fer et empêcher toute corrosion future. Il est commercialisé en tant que convertisseur de rouille[10].
Notes et références
modifier- Acide tannique« Acide tannique » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 07/07/2009
- The Merck Index, 9th edition, Merck & Co., Rahway, New Jersey, 1976
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) MSDS for tannic acid
- Acide tannique-granulat [PDF]
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur monographs.iarc.fr, CIRC, (consulté le ).
- « tanins », sur ESIS, consulté le 07/07/2009
- Cf. Jöns Jakob Berzelius, Olof Gustaf Öngren et A. Wahlen et al., Traité de chimie, vol. 2, Paris, Firmin Didot et Fr.,
- (en) John Aurie Dean, Norbert Adolph Lange, Lange's handbook of chemistry, McGraw-Hill, , 15e éd., 1424 p. (ISBN 0-07-016384-7), p. 11.67
- « Convertisseur de rouille », Soudal, (consulté le ).
Voir aussi
modifierArticles connexes
modifier- Tanin
- Liste d'acides
- « E181 », sur OpenFoodFacts.
