Acide 2-aminomuconique-6-semialdéhyde
composé chimique
L’acide 2-aminomuconique-6-semialdéhyde est un composé chimique de formule HOOC–C(NH2)=CH–CH=CH–CHO. C'est un métabolite de la dégradation du tryptophane chez les mammifères. Il intervient dans la voie de la kynurénine, laquelle prend place dans la biosynthèse du NAD+ chez tous les eucaryotes.
| Acide 2-aminomuconique-6-semialdéhyde | |
 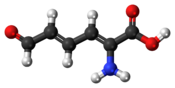 Structure de l'acide 2-aminomuconique-6-semialdéhyde |
|
| Identification | |
|---|---|
| Nom UICPA | acide 2-amino-6-oxohexa-2,4-diénoïque |
| No CAS | |
| PubChem | 30 |
| ChEBI | 15745 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C6H7NO3 [Isomères] |
| Masse molaire[1] | 141,124 7 ± 0,006 4 g/mol C 51,06 %, H 5 %, N 9,93 %, O 34,01 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'acide 2-aminomuconique-6-semialdéhyde est converti en acide 2-aminomuconique par l'aminomuconate-semialdéhyde déshydrogénase (EC ), faute de quoi il se transforme spontanément en acide picolinique.
Notes et références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Human Metabolome Database « Showing metabocard for 2-Aminomuconic acid semialdehyde (HMDB01280) »
- (en) Z. He et J. C. Spain, « Preparation of 2-aminomuconate from 2-aminophenol by coupled enzymatic dioxygenation and dehydrogenation reactions », Journal of Industrial Microbiology & Biotechnology, vol. 23, no 2, , p. 138-142 (lire en ligne) DOI 10.1038/sj.jim.2900705
- (en) Keri L. Colabroy et Tadhg P. Begley, « Tryptophan Catabolism: Identification and Characterization of a New Degradative Pathway », Journal of Bacteriology, vol. 187, no 22, , p. 7866-7869 (lire en ligne) DOI 10.1128/JB.187.22.7866-7869.2005
- (en) Arata Ichiyama, Shigenobu Nakamura, Hitoshi Kawai, Tasuku Honjo, Yasutomi Nishizuka, Osamu Hayaishi et Siro Sesoh, « Studies on the Metabolism of the Benzene Ring of Tryptophan in Mammalian Tissues – II. Enzymic Formation of α-aminomuconic acid from 3-hydroxyanthranilic acid », The Journal of Biological Chemistry, vol. 240, no 2, , p. 740-749 (lire en ligne)