2,2-Diméthylpropane
Le 2,2-diméthylpropane, généralement appelé néopentane, est un alcane ramifié de formule brute C5H12 et qui peut être représenté par la formule semi-développée C(CH3)4.
| Néopentane | |
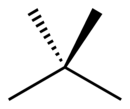  Structure du néopentane |
|
| Identification | |
|---|---|
| Nom UICPA | 2,2-Diméthylpropane[1] |
| Nom systématique | 2,2-Diméthylpropane |
| Synonymes |
néopentane |
| No CAS | |
| No ECHA | 100.006.677 |
| No CE | 207-343-7 |
| No RTECS | LS-120258 |
| PubChem | 10041 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C5H12 [Isomères] |
| Masse molaire[2] | 72,148 8 ± 0,004 8 g/mol C 83,24 %, H 16,76 %, |
| Propriétés physiques | |
| T° fusion | −16,6 °C [3] |
| T° ébullition | 9,5 °C [3] |
| Paramètre de solubilité δ | 12,9 MPa1/2 (25 °C)[4] |
| T° d'auto-inflammation | 450 °C [3] |
| Limites d’explosivité dans l’air | 1,3–7,5 %vol 40–230 g·m-3 [3] |
| Pression de vapeur saturante | 1,456 bar à 20 °C 2,1 bar à 30 °C 3,7 bar à 50 °C [3] |
| Point critique | 160,6 °C, 32 bar, 0,307 l.mol-1 [3] |
| Point triple | 0,355 bar à −16,38 °C [3] |
| Thermochimie | |
| S0liquide, 1 bar | 216,81 J·mol-1·K-1 [5] |
| ΔfH0gaz | −167,9 kJ·mol-1 [5] |
| ΔfH0liquide | −190,3 kJ·mol-1 [5] |
| ΔvapH° | 22,39 kJ·mol-1 à 25 °C 22,74 kJ·mol-1 à 9,55 °C [5] |
| Cp | 120,82 J·mol-1·K-1 (25 °C, gaz) 153,09 J·mol-1·K-1 (−13,22 °C, liquide) [5] |
| Précautions | |
| SGH[7] | |
| H220 et H411 |
|
| SIMDUT[8] | |
  A, B1, |
|
| NFPA 704 | |
| Transport | |
| Écotoxicologie | |
| Seuil de l’odorat | bas : 400 ppm[9] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
C'est, avec le n-pentane et l'isopentane, l'un des trois isomères structuraux du pentane.
Il s'agit d'un gaz hautement inflammable qui peut se condenser aisément en un liquide très volatil.
Nomenclature
modifierLe terme « néopentane » est le nom généralement accepté, et était, au moins jusqu'en 1993, le terme recommandé par l'IUPAC[10],[11]. Les recommandations de 2013[1] semblent avoir évolué sur ce point, recommandent à présent le nom systématique de « 2,2-diméthylpropane », bien que les numéros de substituants soient superflus étant donné que le 2,2-diméthylpropane est le seul « diméthylpropane » possible.
Le groupe néopentyle, souvent noté « Np » — ce qui peut porter à confusion avec l'élément neptunium (numéro atomique 93) aussi noté Np —, a une structure en Me3C–CH2. On le retrouve par exemple dans le néopentanol/2,2-diméthyl-1-propanol (Me3CCH2OH ou NpOH).
On peut également trouver, en particuliers dans des sources plus anciennes, le nom aujourd'hui obsolète de « tétraméthylméthane »[12],[13].
Notes et références
modifier- Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book), Cambridge, The Royal Society of Chemistry, (ISBN 978-0-85404-182-4, DOI 10.1039/9781849733069-FP001), « Front Matter », p. 652
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « 2,2-Dimethylpropane » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 20 avril 2009 (JavaScript nécessaire)
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 978-0-387-69002-5 et 0-387-69002-6, lire en ligne), p. 294
- (en) « Propane, 2,2-dimethyl- », sur NIST/WebBook
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 2, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 0-88415-858-6)
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Néopentane » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- « Neopentane », sur hazmap.nlm.nih.gov (consulté le )
- Table 19(a) Acyclic and monocyclic hydrocarbons. Parent hydrocarbons
- Panico, R. et Powell, W. H., A Guide to IUPAC Nomenclature of Organic Compounds 1993, Oxford, Blackwell Science, (ISBN 978-0-632-03488-8)
- Frank C. Whitmore et Geo. H. Fleming, « Preparation of Tetramethylmethane (Neopentane) and Determination of its Physical Constants1 », Journal of the American Chemical Society, vol. 55, no 9, , p. 3803–3806 (ISSN 0002-7863, DOI 10.1021/ja01336a058)
- Lucien J. B. LaCoste, « The Rotational Wave Equation of Tetramethylmethane for Zero Potential and a Generalization », Physical Review, vol. 46, no 8, , p. 718–724 (DOI 10.1103/PhysRev.46.718, Bibcode 1934PhRv...46..718L)







